
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.1.0 mol·L-1的CaCl2溶液:Na+、K+、Cl-、CO32-
B.1.0 mol·L-1的HNO3溶液:K+、[Ag(NH3)2]+、Cl-、SO42-
C.1.0 mol·L-1的KI溶液:Na+、Fe3+、Cl-、SO42-
D.澄清透明的溶液:Cu2+、SO42-、Mg2+、Cl-
科目:高中化学 来源:2015-2016学年河南省三门峡市高一上学期期中测试化学试卷(解析版) 题型:实验题
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子形式存在。实验室从海藻中提取碘的流程如下:
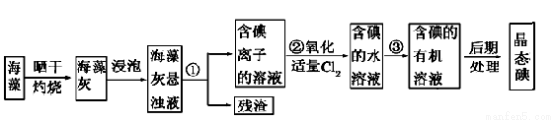
(1)指出提取碘的过程中有关实验操作的名称:
①为 ,③为 ;过程②中有关反应的离子方程式是 。
(2)提取碘的过程中可供选择的有机溶剂是( )
A.甲苯、酒精 B.四氯化碳、苯
C.汽油、醋酸 D.汽油、酒精
(3)为使海藻灰中碘离子转化为碘的有机溶液,实验室里有烧杯、玻璃棒、 集气瓶、酒精灯、导管、圆底烧瓶、石棉网,以及必要的夹持装置、物品,尚缺少的玻璃仪器是 。
(4)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏。指出下图所示的实验装置中的错误之处: ① ,② 。

(5)海藻灼烧时需要的主要仪器是 (填写仪器名称)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省济宁市兖州区高二上学期期中测试化学试卷(解析版) 题型:填空题
(2013秋•兰山区期中)二甲醚(CH3OCH3)和甲醇(CH3OH)被称为21世纪的新型燃料.以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下:
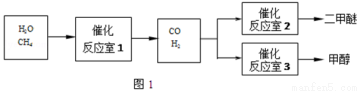
请填空:
(1)一定条件下,反应室1中发生反应CH4(g)+H2O(g)═CO(g)+3H2(g)△H>0.其它条件不变,只降低温度,逆反应速率将 (填“增大”、“减小”或“不变”).
(2)图1中反应室3(容积可变的密闭容器)中0.2mol CO与0.4mol H2在催化剂作用下发生可逆反应生成甲醇:CO(g)+2H2(g) CH3OH(g),CO的平衡转化率与温度、压强的关系如图2所示,则:
CH3OH(g),CO的平衡转化率与温度、压强的关系如图2所示,则:
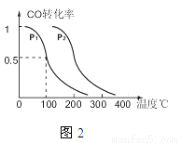
①P1 P2 (填“<”、“>”或“=”).
②在压强P1下,100℃时反应达到化学平衡,反应室3的容积变为2L,此时CO平衡常为 , 若温度不变,再加入1.0mol CO后重新达到平衡,CO的平衡转化率 (填“增大”、“不变”或“减小”).
③保持容积为2L不变,温度100℃不变,向反应室3中再通入0.2mol CO与0.4mol H2,CO的平衡转化率 (填“增大”、“不变”或“减小”).
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二上学期期中测试化学试卷(解析版) 题型:选择题
将反应Cu(s)+2Ag+(aq)===Cu2+(aq)+2Ag(s)设计成原电池,某一时刻的电子流向及电流计(G)指针偏转方向如图所示,下列有关叙述正确的是:
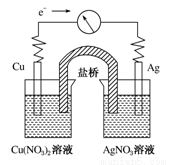
A、KNO3盐桥中的K+移向Cu(NO3)2溶液
B、Cu作负极,发生还原反应
C、电子由AgNO3溶液通过盐桥移向Cu(NO3)2溶液
D、工作一段时间后,AgNO3溶液中c(Ag+)减小
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省淄博市高二上学期期中测试化学试卷(解析版) 题型:选择题
在体积一定的密闭容器中给定物质A、B、C的量,在一定条件下发生反应建立的化学平衡:aA(g) + bB(g) xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图中,Y轴是指
xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图中,Y轴是指
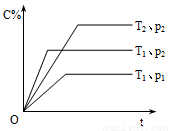
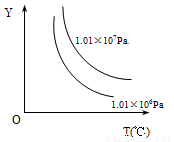
A.反应物A的转化率 B.平衡混合气中物质B的百分含量
C.平衡混合气的密度 D.该反应的正方向的∆H>0
查看答案和解析>>
科目:高中化学 来源:2016届福建省厦门市高三上学期期中测试化学试卷(解析版) 题型:选择题
常温下,向饱和氯水中逐滴滴入0.1mol·L-1的氢氧化钠溶液,pH变化如右图所示,下列有关叙述正确的是

A.①点所示溶液中只存在HClO的电离平衡
B.①到②水的电离程度逐渐减小
C.I-能在②点所示溶液中存在
D.②点所示溶液中:c(Na+)=c(Cl-) + c(ClO-)
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省天水市高三上学期第三次测试化学试卷(解析版) 题型:选择题
下列变化过程不涉及氧化还原反应的是
A.将一小块钠放在石棉网上加热,生成淡黄色物质
B.向新制氯水中加入足量亚硫酸钠溶液,氯水褪色
C.向纯碱溶液中滴加酚酞,溶液变红色
D.向氢碘酸中滴加FeCl3溶液,产生棕色物质
查看答案和解析>>
科目:高中化学 来源:2016届江苏省盐城市高三上学期期中测试化学试卷(解析版) 题型:填空题
K4[Fe(CN)6]强热可发生反应:3 K4[Fe(CN)6] 2 (CN)2↑+12 KCN +N2↑+ Fe3C + C
2 (CN)2↑+12 KCN +N2↑+ Fe3C + C
(1)K4[Fe(CN)6]中Fe2+的配位数为 (填数字);Fe2+基态核外电子排布式为 。
(2)(CN)2分子中碳原子杂化轨道类型为 ;1mol(CN)2分子中含有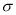 键的数目为 。
键的数目为 。
(3)O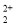 与CN
与CN 互为等电子体,则O
互为等电子体,则O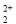 的电子式为 。
的电子式为 。
(4)Fe3C的晶胞结构中碳原子的配位数为6,碳原子与紧邻的铁原子组成的空间构型为 。
查看答案和解析>>
科目:高中化学 来源:2016届山东省临沂市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列物质分类的正确组合是
选项 | 碱 | 酸 | 盐 | 酸性氧化物 |
A | 纯碱 | 盐酸 | 烧碱 | 二氧化硫 |
B | 烧碱 | 硫酸 | 食盐 | 一氧化碳 |
C | 氨水 | 醋酸 | 石灰石 | 水 |
D | 苛性钾 | 碳酸 | 胆矾 | 三氧化硫 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com