
| A. | ①② | B. | ②③④ | C. | ②④ | D. | ①③ |
分析 ①构造原理揭示的电子排布能级顺序,实质是各能级能量高低顺序,原子轨道充满或半充满时原子的能量处于最低状态不遵循构造原理;
②根据构造原理的能量顺序判断;
③pX、pY、pZ轨道能量相同;
④能量最低,最稳定.
解答 解:①原子的电子排布遵循构造原理能使整个原子的能量处于最低状态,但轨道充满或半充满时,能量较小,如Cu:3d104s1,Cr:3d54s1,不遵循构造原理,故①错误;
②3d轨道的能量大于4s轨道的能量,所以4s轨道的能量一定比3d轨道的能量低,故②正确;
③同一电子层中的不同p轨道的能量相同,故③正确;
④原子的电子排布遵循构造原理能使整个原子的能量处于最低状态,故④正确;
故选:B.
点评 本题考查核外电子排布规律,注意构造原理的应用,注重基础知识的考查,题目难度不大.


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:解答题
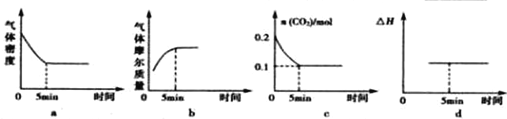
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
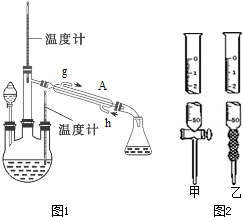
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由硫酸铁溶液与硫酸铵溶液按一定比例混合后蒸发结晶而得 | |
| B. | 此溶液中与下列粒子可以大量共存:H+、SO42-、I-、C6H5OH | |
| C. | 此溶液中离子浓度大小关系为:SO42->Fe3+>H+>OH- | |
| D. | 将含0.1 molNH4Fe(SO4)2溶液中滴加0.1 molBa(OH)2,反应的离子方程式为:Fe3++2SO42-+2Ba2++3OH-=2BaSO4↓+Fe(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
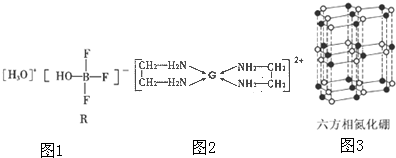
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝基苯、苯、乙醇三种液体 | B. | 硫酸钠、硝酸钾、氯化钡三种固体 | ||
| C. | 硫磺、过氧化钠、氯化钙三种固体 | D. | 氯化铝、偏铝酸钠、烧碱三种固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10℃20 mL 3mol/L的X溶液 | B. | 20℃30 mL 2molL的X溶液 | ||
| C. | 20℃10 mL 4mol/L的X溶液 | D. | 10℃10 mL 2mol/L的X溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
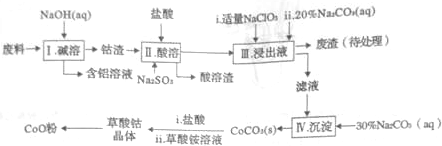
| Fe3+ | Co2+ | Co3+ | Al2+ | |
| pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
| pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
| 温度范围/℃ | 固体质量/g |
| 150~210 | 4.41 |
| 290~320 | 2.41 |
| 890~920 | 2.25 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com