
关于下列各装置图的叙述中,正确的是 
| A.若采用装置①精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液 |
| B.装置②是原电池,能将化学能转化为电能,锌电极发生还原反应 |
| C.装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸 |
| D.装置④可用于收集氨气,并吸收多余的氨气 |
科目:高中化学 来源: 题型:单选题
如图为铁片上镀铜的实验装置,下列说法正确的是
| A.Cu2+在A极被还原 |
| B.硫酸铜溶液浓度变小 |
| C.铜片连接电源正极,铁片上发生还原反应 |
| D.B极发生反应:Cu-2e-=Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下图是水煤气(成分为CO、H2)、空气燃料电池的工作原理示意图,a、b均为惰性电极。下列叙述中正确的是
| A.A处通入的是空气,B处通入的是水煤气 |
| B.a电极发生还原反应,b电极发生氧化反应 |
| C.如用这种电池电镀铜,待镀金属增重6.4 g,则至少消耗标准状况下的水煤气2.24 L |
| D.a电极的反应式包括:CO+4OH-+2e-=CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述正确的是
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③电镀时,应把镀件置于电解槽的阴极
④冶炼铝时,用电解熔融氧化铝的方法
⑤钢铁表面常易锈蚀生成Fe2O3?nH2O
| A.①②③④⑤ | B.①③④⑤ | C.①③⑤ | D.②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述正确的是
| A.纯锌与硫酸反应时,加入少量CuSO4溶液,可使反应速率加快 |
| B.甲醇和氧气以及KOH溶液构成的新型燃料电池中,其负极上发生的反应为:CH3OH+6OH- +6e-=CO2 +5H2O |
| C.在铁件上镀铜时,金属铜作阴极 |
| D.电解精炼铜时电解质溶液中铜离子浓度保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用惰性电极电解某金属元素R的硝酸盐R(NO3)n溶液,通电一段时间后,阳极产生气体V L(标准状况)时,阴极质量增加m g,若R的相对原子质量为M,设NA为阿伏加德罗常数的值,下列叙述中不正确的是
A.电路中通过电子 NA NA | B.n =  |
C.溶液中H+增加 NA NA | D.n =  |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关金属腐蚀与防护的说法正确的是
| A.纯银器表面在空气中会因化学腐蚀渐渐变暗 |
| B.地下输油钢管与外加直流电源的正极相连可保护其不受腐蚀 |
| C.海轮外壳连接锌块是采用牺牲阴极的阳极保护法保护外壳不受腐蚀 |
| D.当镀锡铁制品的镀层破损时,锡镀层仍能对铁制品起保护作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法错误的是( )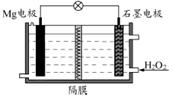
| A.Mg 电极是该电池的负极 |
| B.溶液中Cl-向石墨电极移动 |
| C.该装置中电子从Mg电极流向石墨电极 |
| D.H2O2在石墨电极上发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应
Cr2O72–+6Fe2++14H+ 2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法不正确的是
2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法不正确的是
A.阳极反应为Fe-2e- Fe2+ Fe2+ |
| B.电解过程中溶液pH不会变化 |
| C.反应过程中有Fe(OH)3沉淀生成 |
| D.电路中每转移12 mol电子,最多有1 mol Cr2O72-被还原 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com