
分析 (1)铝在酒精灯火焰上加热,铝表面生成氧化铝,氧化铝的熔点高于铝,所以内部的铝熔化;
(2)铝与水不反应,钠与水迅速反应产生氢气;生成的氢氧化钠溶液又溶解金属铝再产生氢气.相关的化学方程式为:2Na+2H2O=2NaOH+H2↑; 2Al+2NaOH+2H2O=2 NaAlO2+3H2↑;
(3)用砂纸打磨铝片,表面的氧化铝被除去,铝与硫酸铜溶液反应置换出铜;
(4)氧化铝与氢氧化钠反应生成盐和水;
(5)开始时浓氢氧化钠溶液吸收CO2引起易拉罐内压强减小,导致易拉罐变瘪,离子方程式为:CO2+2OH-=CO32-+H2O;过一会后暴露出来的Al又与氢氧化钠溶液反应生成了H2,压强又逐渐增大,导致易拉罐又重新鼓了起来.
解答 解:(1)铝在酒精灯火焰上加热,铝表面生成氧化铝,氧化铝的熔点高于铝,所以内部的铝熔化,但外面的氧化铝并不熔化,好象有一层膜兜着,故答案为:高于;
(2)铝包在钠表面,铝与水不反应.用针刺些小孔后钠与水生成氢氧化钠和氢气,生成的氢氧化钠溶液又与铝产生氢气.反应方程式为2Na+2H2O=2NaOH+H2↑; 2Al+2 NaOH+2H2O=2 NaAlO2+3H2↑,故答案为:2Na+2H2O=2NaOH+H2↑; 2Al+2 NaOH+2H2O=2 NaAlO2+3H2↑;
(3)用砂纸打磨铝片,表面的氧化铝被除去,铝与硫酸铜溶液反应置换出铜,化学方程式为:2Al+3Cu2+=2Al3++3Cu,故答案为:2Al+3Cu2+=2Al3++3Cu;
(4)氧化铝与氢氧化钠反应生成偏铝酸钠和水,离子方程式为Al2O3+2OH-=2AlO2-+H2O,故答案为:Al2O3+2OH-=2AlO2-+H2O;
(5)开始时浓氢氧化钠溶液吸收CO2引起易拉罐内压强减小,导致易拉罐变瘪,离子方程式为:CO2+2OH-=CO32-+H2O;过一会后暴露出来的Al又与氢氧化钠溶液反应生成了H2,压强又逐渐增大,导致易拉罐又重新鼓了起来,离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑.
点评 对于此类信息给予题,要结合所学知识,认真分析,抓住有用信息,大胆猜测,利用所有知识进行验证,从而得出正确结论.


科目:高中化学 来源: 题型:选择题
| A. | 该溶液的pH一定等于1 | |
| B. | 阴离子肯定有I-,不能确定有无HCO3- | |
| C. | 阳离子肯定没有Fe3+,可能有Na+ | |
| D. | 该溶液含有的溶质成分可能为HI或HI和NaI或NaI和NaOH或NaI |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 $→_{△}^{-H_{20}}$CH3CH=CHCHO,水杨酸酯E为紫外线吸收剂,可用于配制防晒霜.E的一种合成路线如下:
$→_{△}^{-H_{20}}$CH3CH=CHCHO,水杨酸酯E为紫外线吸收剂,可用于配制防晒霜.E的一种合成路线如下:
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(l)△H=+817.63 kJ•mol-1 | |
| B. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.63 kJ•mol-1 | |
| C. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(l)△H=-641.63 kJ•mol-1 | |
| D. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-817.63 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 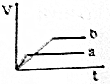 | B. | 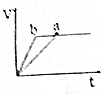 | C. |  | D. | 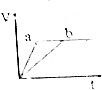 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
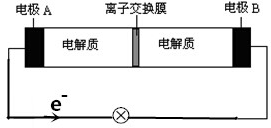
| A. | 放电时,Na+从右到左通过离子交换膜 | |
| B. | 放电时,负极反应式为3NaBr-2e-═NaBr3+2Na+ | |
| C. | 充电时,A极应与直流电源负极相连 | |
| D. | 放电时,当有0.1molNa+通过离子交换膜时,B极上有0.3molNaBr产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加热 | B. | 使用催化剂 | C. | 加压 | D. | 分离出D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com