
����Ŀ������þ[Mg(ClO3)2]����������������ݼ��ȣ�ʵ�����Ʊ�����Mg(ClO3)2��6H2O����������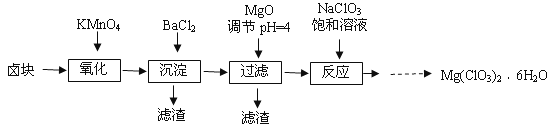
��֪����±����Ҫ�ɷ�ΪMgCl2��6H2O������MgSO4��FeCl2�����ʡ�
�����ֻ�������ܽ��(S)���¶�(T)�仯������ͼ��ʾ��
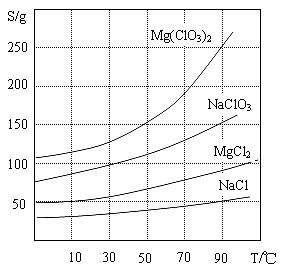
��1����������Ҫ����Ҫ���������� ��
��2������BaCl2��Ŀ���� ����MgO�����������������Ҫ�ɷ�Ϊ ��
��3������NaClO3������Һ������Ӧ�Ļ�ѧ����ʽΪ ���ٽ�һ����ȡMg(ClO3)2��6H2O��ʵ�鲽������Ϊ���������ᾧ���� ��ϴ�ӣ�������Һ��ȴ�ᾧ�������ˡ�ϴ����
��4����Ʒ��Mg(ClO3)2��6H2O�����IJⶨ������֪Mg(ClO3)2��6H2O��Ħ������Ϊ299g/mol��
����1��ȷ����3.50 g��Ʒ���100 mL��Һ��
����2��ȡ10.00 mL����ƿ�У�����10.00 mLϡ�����20 .00mL 1.000 mol��L��1��FeSO4��Һ���ȡ�
����3����ȴ�����£���0.100 mol/L K2Cr2O7 ��Һ�ζ�ʣ���Fe2+���յ㡣��Ӧ�ķ���ʽΪ: Cr2O72-��6Fe2+��14H+��2Cr3+��6Fe3+��7H2O��
����4��������2��3�ظ����Σ�ƽ������K2Cr2O7 ��Һ15.00 mL��
��д������2�з�����Ӧ�����ӷ���ʽ�� ��
�� ��Ʒ��Mg(ClO3)2��6H2O����������Ϊ ����������С�����һλ��
���𰸡���1��©�������������ձ�����2����ȥSO42- �� ʹSO42-������Fe(OH)3��
��3��MgCl2��2NaClO3��Mg(ClO3)2��2NaCl�������ȹ��ˣ�
��4����ClO3�� ��6Fe2����6H����6Fe3����Cl����3H2O����78.3%��
��������
�����������1������ʹ����������©�����ձ�������������ֽ��������Ȧ������̨����˲��������ǣ�©�����ձ�����������
��2�����ݺ������ʣ���˼���BaCl2��Һ����Ba2����SO42��=BaSO4���������dz�ȥSO42����ʹSO42����������������Ŀ�ģ���˼���MgO����pHʹFe3��ȫ��ת����Fe(OH)3����������ijɷ���Fe(OH)3��
��3�������ܽ�����¶ȱ仯���ߣ��ܽ�ȴ��ת�����ܽ��С������NaClO3������Һ�����ķ�Ӧ��2NaClO3��MgCl2=Mg(ClO3)2��2NaCl������Ϊ�õ���Mg(ClO3)2��6H2O����˲��ü������������ȹ��ˣ�
��4����ClO3�����������ԣ��ܰ�Fe2��������Fe3�������ݻ��ϼ�������������ƽ��������ӷ�Ӧ����ʽ��6Fe2����ClO3����6H��=6Fe3����Cl����3H2O��������3�ó�����2��ʣ���n(Fe2��)=6��15��10��3��0.1mol=9��10��3mol����n(ClO3��)=(20��10��3��1��9��10��3)/6mol=1.1��10��2/6mol�������Ʒ��m[Mg(ClO3)2��6H2O]=1.1��10��2��100��299/(10��2��6) g=2.74g����������Ϊ2.74/3.5��100%=78.3%��


 �ǻ�С��ϰϵ�д�
�ǻ�С��ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������ک�100��ĵ����ºϳ�һ����X���˷��ӵ�ģ����ͼ��ͼ�е����߱�ʾ��ѧ����������˵����ȷ���ǣ� �� 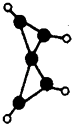
A.X��ʹ������Ȼ�̼��Һ��ɫ
B.X��һ���ڳ��������ȶ����ڵ�Һ̬��
C.X��������ͬһƽ���ϵ�̼ԭ�����5��
D.���ȼ�յ�������X�ͼ��飬X����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Na2O��NaOH��Na2CO3��NaCl��Na2SO4�ɰ�ij�ֱ�����Ϊͬһ�����ʣ����з������ȷ����
���ƵĻ����� ���������ᷴӦ������ �۵���� ������ ���Ƶĺ���������
A���٢� B���ۢ� C���ڢ� D���٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���طŵ硢���ʱ�ķ�ӦΪFe+Ni2O3+3H2O ![]() Fe��OH��2+2Ni��OH��2�����ƶ��в���ȷ���ǣ� �� �ٷŵ�ʱ��FeΪ������Ni2O3Ϊ����
Fe��OH��2+2Ni��OH��2�����ƶ��в���ȷ���ǣ� �� �ٷŵ�ʱ��FeΪ������Ni2O3Ϊ����
�ڳ��ʱ�������ϵĵ缫��Ӧʽ��Fe��OH��2+2e���TFe+2OH��
�۳��ʱ��Ni��OH��2Ϊ����
�����صĵ缫�����ǽ���ij�ּ��Ե������Һ�У�
A.��
B.�٢ڢ�
C.�٢ۢ�
D.�ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��F��G��H����Ԫ�طֲ���������ͬ�Ķ����ڣ����ǵ�ԭ������������������B��C��DΪͬһ���ڣ�A��E��B��G��D��H�ֱ�Ϊͬһ���壬C��D������������֮��Ϊ11��C��D��F����Ԫ�ص�ԭ������֮��Ϊ28����ش��������⣺
��1��B��D���γɹ��ۻ�����X��������X��F D2����Һ��Ӧ�����ӷ���ʽΪ____________________________
��2��E��F��H���γɵļ����ӵİ뾶�ɴ�С��˳��Ϊ�������ӷ��ű�ʾ��_________��
��3��G�������������B�ĵ����ڸ������ܷ����û���Ӧ���仯ѧ��Ӧ����ʽΪ��
____________________________________________________��
��4����Y��B��D��E��ɡ���������YΪ����ʹ��ɵ�����ȼ�ϵ�ء�д��ʯī�����Ϸ����ĵ缫��Ӧʽ��________________________________��
��5��1gҺ̬A4BDȼ��ͨ������·ų�13.86KJ������д��������ȼ���ȵ��Ȼ�ѧ����ʽ��_________________________________________________________________
��6����һ��װ�п��ƶ������������н������·�Ӧ��C2��g����3A2��g��![]() 2CA3��g������Ӧ�ﵽƽ���������к���C2��0.5mol��A20.2mol��CA30.2mol�����ݻ�Ϊ1.0L��
2CA3��g������Ӧ�ﵽƽ���������к���C2��0.5mol��A20.2mol��CA30.2mol�����ݻ�Ϊ1.0L��
�������ɴ�ƽ��ǰ��������ʼ���������¼��ֿ��ܣ����в���������________��
A��C2��0.6mol�� A2��0.5mol�� CA30mol
B��C2 0mol�� A2��0mol�� CA3��1.2mol
C��C2��0.6mol/L��A2��0.5mol/L�� CA3��0.1mol/L
�������ƽ����ϵ��ƽ�ⳣ��K��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ����ʱ��ʹ�ú��γ�һ��ˮ������Ҫ�ɷ�ΪCaCO3���������е��������ʿ��������ˮ�����ǣ�������
A.�״�
B.ʳ��
C.�Ͼ�
D.С�մ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ�������ΪVa��pH=a��ijһԪ�������Vb��pH=b��ijһԪ���ϣ���������и��⣮
��1����a+b=14��2Va=Vb �� ����NaOH����Ӧ��������ҺpHС��7���ɴ����ܵõ��Ľ����� ��
��2����a+b=13���������ᣬ����b=12��KOH����������ζ�50.00mL KOH��Һ�����ζ�����Һ��pH=2ʱ��������������V=mL��
��3������֪Va��Vb��a=0.5b������ǿ�ᣬ����ǿ���ͼ�ǡ���кͣ���a��ȡֵ��Χ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵķ�����ȷ����(����)
ѡ�� | �� | �� | �� | ���������� | ���������� |
A | Na2CO3 | H2SO4 | NaOH | SO2 | CO2 |
B | NaOH | HCl | NaCl | Na2O | NO |
C | KOH | HNO3 | CaCO3 | CaO | Mn2O7 |
D | NaOH | HCl | CaF2 | Na2O2 | SO2 |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ӷ���ʽBaCO3��2H��===CO2����H2O��Ba2���е�H�����ܴ�����������( )
��HCl����H2SO4����HNO3����NaHSO4����CH3COOH
A. �٢� B. �٢ܢ� C. �٢� D. �ڢܢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com