
纯碱一直以来都是工业生产的重要原料,很长一段时间来纯碱的制法都被欧美国家所垄断。上个世纪初我国著名的工业化学家侯德榜先生,经过数年的反复研究终于发明了优于欧美制碱技术的联合制碱法(又称侯氏制碱法)。并在天津建造了我国独立研发的第一家制碱厂。其制碱原理的流程如图所示:
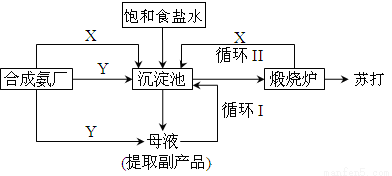
(1)侯德榜选择天津作为制碱厂的厂址有何便利条件(举二例说明)_____________、______________。
(2)侯氏制碱法的最终产物是(化学式)_______________;其在水溶液中显著的实质是(离子方程式):__________________。
(3)合成氨工厂需要向制碱厂提供两种原料气体,它们分别是:______________、_____________。这两种气体在使用过程中是否需要考虑添加的顺序?____________(填“是”或“否”),原因是_______________。
(4)在沉淀池中发生的反应的化学方程式是_________________。
(5)使原料水中溶质的利用率从70%提高到90%以上,主要是设计了_____________(填上述流程中的编号)的循环.从母液中可以提取的副产品的应用是______________(举一例)。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2016届湖北省高三普通班8月月考化学试卷(解析版) 题型:选择题
下列化学用语正确的是:
A .乙烯的结构式:CH2=CH2
B.Clˉ的结构示意图: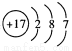
C.I—131:78 53I
D.Na2S 的电子式: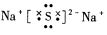
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高一上期中测试化学试卷(解析版) 题型:选择题
为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作,其中正确的操作顺序是
①过滤 ②加过量的NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液
A.①④②⑤③ B.④①②⑤③ C.④②⑤①③ D.⑤②④①③
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃兰州一中高二上期中测试理科化学试卷(解析版) 题型:计算题
(12分)在2L密闭容器中,充入1 mol N2和3mol H2,一定条件下发生合成氨反应,2min时达到平衡。测得平衡时N2的转化率为40%,求:
(1)平衡时v (NH3)的速率
(2)求该温度下的平衡常数K(列出算式,不用计算出结果)
(3)H2在平衡混合气体中的体积分数
(4)平衡时容器的压强与起始时压强之比
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期10月月考化学试卷(解析版) 题型:选择题
海水开发利用的部分过程如图所示。下列说法错误的是
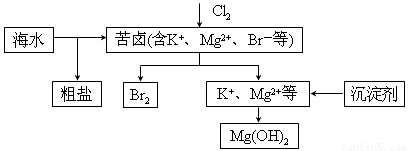
A.向苦卤中通入Cl2是为了提取溴
B.粗盐可采用除杂和重结晶等过程提纯
C.工业生产中常选用NaOH作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济南外国语学校高三上学期期中测试化学试卷(解析版) 题型:选择题
在pH为3的FeCl3溶液,pH为11的Na2CO3溶液和pH为3的盐酸中由水电离出来的H+的浓度分别为:C1、C2、C3它们之间的关系是
A.C1<C2<C3 B.C1=C2>C3 C.C1>C2>C3 D.无法判断
查看答案和解析>>
科目:高中化学 来源:2016届山东省南校区高三上学期10月阶段测化学试卷(解析版) 题型:选择题
某无色透明溶液能与铝粉反应放出H2,则此溶液中可能存在
A.OH-、Ba2+、Cl-、Na+ B.H+、Cl-、Na+、SO42-
C.H+、Cu2+、[Al(OH)4]-、SO42- D.H+、Ba2+、Mg2+、NO3-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁实验中学高一上10月阶段测化学试卷(解析版) 题型:选择题
阿佛加德罗常数为6?02×1023 mol?1。下列叙述中不正确的是
A.0.1 mol OH-含有6?02×1023 个电子
B.氯化氢气体的摩尔质量等于6?02×1023个氯化氢分子的质量之和
C.1 mol醋酸的质量与6?02×1023个醋酸分子的质量相等
D.28 g氮气所含的原子数目为12?04×1023
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上学期第一次月考化学试卷(解析版) 题型:选择题
下列热化学方程式中,正确的是
A.甲烷的燃烧热为890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为:
CH4(g)+2O2(g)==CO2(g)+2H2O(g)△H=-890.3kJ/mol
B.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g)△H=-38.6kJ/mol
2NH3(g)△H=-38.6kJ/mol
C.NaOH(s)+1/2 H2SO4(浓)==1/2Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol
D.2.00gC2H2气体完全燃烧生成液态水和二氧化碳气体,放出99.6kJ的热量,该反应的热化学方程式为:2C2H2(g)+5O2(g)==4CO2(g)+2H2O(l)△H=-2589.6kJ/moL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com