
| A、水的离子积Kw随温度、外加酸(碱)浓度的改变而改变 |
| B、能自发进行的化学反应,一定是△H<0、△S>0 |
| C、当弱电解质电离成离子的速率与离子结合成分子的速率相等时达到电离平衡状态 |
| D、Ksp不仅与难溶电解质的性质和温度有关,还与溶液中的离子浓度有关 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、常温下浓硫酸遇到铝发生钝化,可在常温下用铝制容器贮藏贮运浓硫酸 |
| B、盐析可提纯蛋白质并保持其生理活性 |
| C、二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| D、锌的金属活泼性比铁的强,可在海轮外壳上装若干锌块以减缓其腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、废弃的金属、纸制品、塑料是可回收资源,玻璃不是可回收资源 |
| B、大力推广农作物的生物防治技术,以减少农药的使用 |
| C、“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”都能提高空气质量 |
| D、“低碳生活”倡导生活中耗用能量尽量减少从而减少CO2排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应NH3(g)+HCl(g)=NH4Cl(s)低温下能自发进行,说明该反应的△H<0 |
| B、反应N2(g)+3H2(g)=2NH3(g)(△H<0)达平衡后,降低温度,正反应速率增大、逆反应速率减小,平衡向正反应方向移动 |
| C、Mg在空气中燃烧时发出耀眼的白光,可用于制造信号弹 |
| D、纯碱溶于热水中去污效果增强,说明纯碱的水解是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、凡是生成盐和水的反应都是中和反应 |
| B、复分解反应可能是氧化还原反应 |
| C、生成一种单质和一种化合物的反应一定是置换反应 |
| D、有单质生成的分解反应一定是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
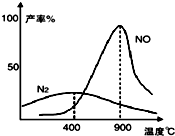 氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如图):
氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如图):查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com