
【题目】下列关于元素金属性、非金属性强弱判断不正确的是( )
A. 高温下2C+SiO2![]() 2CO↑+Si,说明非金属性:C>Si
2CO↑+Si,说明非金属性:C>Si
B. 碱性:KOH>Mg(OH)2,说明金属性:K>Mg
C. 氟气与氢气在暗处相遇就会爆炸,氯气与氢气混合在光照或点燃时发生爆炸,说明非金属性:F>Cl
D. 氧化性:Cu2+>Na+,说明金属性:Na>Cu
科目:高中化学 来源: 题型:
【题目】能证明碳酸的酸性比硅酸强的事实是
A. 二氧化碳溶于水且能反应生成碳酸,二氧化硅不溶于水不能与水反应生成硅酸
B. 在高温下,二氧化硅与碳酸钠能发生反应:SiO2+Na2CO3![]() Na2SiO3+CO2↑
Na2SiO3+CO2↑
C. 二氧化硅的熔点比二氧化碳的熔点高
D. 二氧化碳通入硅酸钠溶液中,生成白色胶状沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】功能高分子P的合成路线如下:

(1)A的分子式是C7H8,其结构简式是________________________。
(2)试剂a是____________________。
(3)反应③的化学方程式:_________________________________________________。
(4)E的分子式是C6H10O2。E中含有的官能团:_________________________。
(5)反应④的反应类型是____________________________。
(6)反应⑤的化学方程式:_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关乙烯分子中的化学键描述正确的是
A. 碳原子的三个sp2杂化轨道与其它原子形成三个σ键
B. 每个碳原子的未参加杂化的2p轨道形成σ键
C. 每个碳原子的sp2杂化轨道中的其中一个形成π键
D. 碳原子的未参加杂化的2p轨道与其它原子形成σ键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铝土矿主要含Al2O3和SiO2。某课题组以此为原料回收氧化铝,设计实验流程如下:
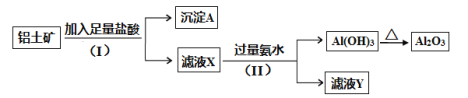
(1)步骤(I)中分离溶液和沉淀的操作名称是_____,实验中除了烧杯和玻璃棒外,还需要用到的玻璃仪器是_____。
(2)沉淀A中一定含有_________(用化学式表示),该物质属于________(填 “酸性”或“碱性”)氧化物。
(3)写出步骤(Ⅱ)中生成Al(OH)3的离子方程式___________________。
(4)实验室里用Na[Al(OH)4]溶液制取Al(OH)3最好选用__________(填序号)。
A.NaOH溶液 B.稀硫酸 C.二氧化碳
(5)取5.4g铝土矿进行实验,最后得到氧化铝5.1g,则该铝土矿中铝的含量为____________(假设实验过程没有损失)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种酸性“二甲醚(CH3OCH3)直接燃料电池”具有启动快、能量密度高、效率好等优点,其电池原理如图所示。下列有关该电池的说法不正确的是
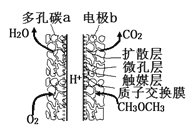
A. 多孔碳a能增大气固接触面积,提高反应速率,该电极为负极
B. 电极b上发生的反应为:CH3OCH3-12e-+3H2O=2CO2+12H+
C. H+由b电极向a电极迁移
D. 二甲醚直接燃料电池能量密度( kW·h·kg-1)约为甲醇(CH3OH)直接燃料电池能量密度的1.4倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2A(g)![]() 2B(g)+C(g)在恒压的密闭容器中反应,下列选项中不能说明反应已达到平衡状态的是( )
2B(g)+C(g)在恒压的密闭容器中反应,下列选项中不能说明反应已达到平衡状态的是( )
A. 容器内气体密度不再改变的状态
B. v(A):v(B):v(C)=2:2:1
C. c(A):c(B):c(C)的值保持不变
D. 混合气体的平均相对分子质量不再改变的状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2H4·H2O(水合肼)极毒且不稳定,100℃以上易分解失水,常用作还原剂和除氧剂(通常生成N2和H2O),其熔点为-40℃,沸点118.5℃。现以Cl2、NaOH、(NH2)2CO(尿素)和SO2为原料可制备N2H4·H2O和无水Na2SO3,其主要流程如下:
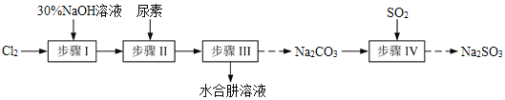
已知:Cl2(g)+2OH-(aq)=ClO-(aq)+Cl-(aq)+H2O(aq) △H<0
(1)配制30%NaOH溶液时,所需玻璃仪器除量筒、烧杯外,还需要_____________(填标号)。
A.容量瓶 B.胶头滴管 C.玻璃棒 D.锥形瓶
(2)步骤Ⅰ制备NaClO溶液时,若温度超过40℃,Cl2与NaOH溶液充分反应生成NaClO3和NaCl。实验中为控制反应温度除了用冰水浴、充分搅拌外,还需采取的措施是_______________________。
(3)步骤Ⅱ合成N2H4·H2O的装置如图1所示。NaClO碱性溶液与尿素水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应。实验中通过滴液漏斗滴加的溶液是_____________(填字母);
a.尿素溶液 b.NaClO碱性溶液 c.尿素溶液或NaClO溶液任选其一
理由是____________________________________。
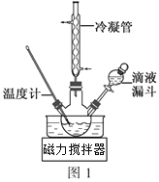
(4)步骤Ⅲ中分离出N2H4·H2O应该采用的方法最合理是____________________。
(5)步骤Ⅳ用步骤Ⅲ得到的副产品Na2CO3制备无水Na2SO3(水溶液中H2SO3、HSO3-、SO32-随pH的分布如图2所示,Na2SO3的溶解度曲线如图3所示)。
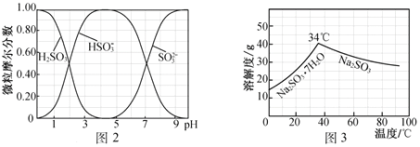
①边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。实验中确定何时停止通SO2的方法是______________。
②请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案:_________________________________,用少量无水乙醇洗涤,干燥,密封包装。
(6)工业上还可以用水合肼还原法制取碘化钠,工艺流程如图:
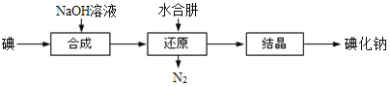
还原过程中可用硫化钠或铁屑等物质替代水合肼,但水合肼还原法制得的产品纯度更高,原因是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH![]() 、Cl-、Mg2+、Ba2+、CO
、Cl-、Mg2+、Ba2+、CO![]() 、SO
、SO![]() ,现取三份100 mL该溶液进行如下实验:
,现取三份100 mL该溶液进行如下实验:
(1) 第一份加入AgNO3溶液有沉淀产生;
(2) 第二份加足量NaOH溶液加热后,收集到气体0.04 mol;
(3) 第三份加足量BaCl2溶液后,干燥后得沉淀6.27 g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g。根据上述实验,以下推测正确的是( )
①K+一定存在;②100 mL溶液中含0.01 mol CO![]() ;③Cl-可能存在;
;③Cl-可能存在;
④Ba2+一定不存在;⑤Mg2+可能存在
A. ③④ B. ③④⑤
C. ①② D. ①③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com