
【题目】常温下,向 1L 0.10 mol·L-1CH3COONa 溶液中,不断通入HC1气体(忽略溶液体积变化),得到 c (CH3COO-)和c(CH3COOH)与 pH 的变化关系如下,则下列说法正确的是
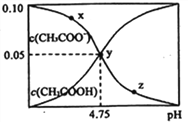
A. 溶液的pH比较:x<y <z
B. 在y点再通入0.05 mol HCl气体,溶液中离子浓度大小比较:
c(Na+) =c(Cl-) > c(H+) >c(CH3COO-) >c(OH-)
C. 在溶液中加入一滴强酸或强碱,溶液pH变化最小的是y点
D. 该温度下,CH3COOH的Ka=104.75
【答案】C
【解析】A.因CH3COO-的水解,CH3COONa 溶液显碱性,通入HCl气体后溶液的碱性逐渐减弱,酸性增强,则pH比较是x>y>z,故A错误;
B.在y点再通入0.05 mol HCl气体,溶液中CH3COONa 和CH3COOH等物质的量混合,因溶液显酸性,说明CH3COOH电离大于CH3COO水解,溶液中离子浓度大小比较关系是c(CH3COO-) >c(Na+) =c(Cl-) > c(H+) >c(OH-),故B错误;C.y点形成了缓冲溶液, 在溶液中加入一滴强酸抑制电离CH3COOH、加入一滴强碱抑制CH3COO-水解,溶液pH变化最小,故C正确;D.y点的溶液中存在CH3COOH![]() CH3COO-+H+ ,溶液中c(CH3COOH) 和c(CH3COO-) 近似相等,CH3COOH的Ka=[c(CH3COO-)×c(H+) ]÷c(CH3COOH) =10-4.75,故D错误;答案为C。
CH3COO-+H+ ,溶液中c(CH3COOH) 和c(CH3COO-) 近似相等,CH3COOH的Ka=[c(CH3COO-)×c(H+) ]÷c(CH3COOH) =10-4.75,故D错误;答案为C。


科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol·L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断错误的是( )
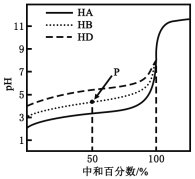
A.三种酸的电离常数关系:KHA>KHB>KHD
B.滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
C.pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)
D.当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )
A. 0.1 mol·L-1MgCl2溶液中含有的Mg2+数目一定小于0.1NA
B. 标准状况下,11.2 L CCl4中含有的分子数目为0.5NA
C. 28 g聚乙烯中含有的碳原子数目为2NA
D. 1 mol CH5+中含有的电子数目为11NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、R、Q、M是六种短周期元素,原子序数依次增大。X是原子半径最小的元素,Y的气态氢化物能使湿润的红色石蕊试纸变蓝,Z为地壳中含量最多的元素,R与X同主族;Y、R、Q最外层电子数之和为8,M的单质黄绿色有害气体。请回答下列问题:
(1)R在元素周期表中的位置为___________。
(2)Z、Q、M简单离子半径由大到小的顺序为(写元素离子符号)___________。
(3)YX4M的电子式为___________,Q3Y2与水可剧烈反应,产生沉淀与气体,反应的化学方程式为____________________。
(4)X、Z两元素形成的原子个数比为1:1的化合物中含有的化学键类型为__________。
(5)M的单质与R的最高价氧化物对应的水化物反应的离子方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校学生小组为探究乙酸、碳酸和苯酚的酸性强弱进行下述实验。该校学生设计了下图的实验装置(夹持仪器已略去)。
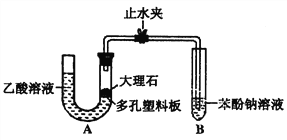
(1)某生检查装置A的气密性时,先关闭止水夹,从左管向U型管内加水,至左管液面高于右管液面,静置一段时间后,若U型管两侧液面差不发生变化,则气密性良好。你认为该生的操作正确与否?_______(填“正确”或“错误”),大理石与乙酸溶液反应的离子方程式为______________。
(2)装置A中反应产生的气体通入苯酚钠溶液中,实验现象为________________反应的离子方程式为_________________
(3)有学生认为(2)中的实验现象不足以证明碳酸的酸性比苯酚强,理由是_______________改进该装置的方法是____________________。
(4)在相同温度下,测定相同物质的量浓度 a.NaHCO3溶液 b.Na2CO3溶液 c. CH3COONa溶液 d. ![]() -ONa溶液的pH, 其pH由大到小排列的顺序为 _______________(填溶液编号)
-ONa溶液的pH, 其pH由大到小排列的顺序为 _______________(填溶液编号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)完全燃烧0.1 mol某烃,燃烧产物依次通过浓硫酸、浓碱液,实验结束后,称得浓硫酸增重9 g,浓碱液增重17.6 g。该烃的化学式为______,并写出其所有可能的结构简式:__________________。
(2)某烷烃的相对分子质量为128,该烷烃的化学式为__________________。
(3)在120 ℃和101 kPa的条件下,某气态烃和一定质量的氧气混合,点燃完全反应后再恢复到原来的温度时,气体体积不变,则该烃分子内的氢原子个数______。
A.小于4 B.大于4
C.等于4 D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种重要的化工原料,其分子组成为C4H9Cl,A有如下转化关系:
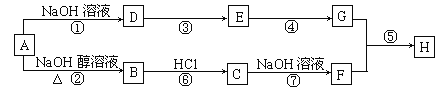
其中F不能发生催化氧化反应,E和G都能和新制Cu(OH)2反应,但反应条件实验现象不同,H是一种有果香味的液体。
(1)A的结构简式为_______________,A的同分异构体有_____种
(2)与①、⑦反应类型相同的是_______(填序号,后同),若A中混有C,则对生成的B的纯度是否有影响______(填“是”或“否”),理由是_____________
(3)写出下列反应的化学方程式:
A→B:__________________;
G+F→H:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用浓度为0.1000mol/L的盐酸分别逐滴加入到20.00mL 0.1000mol/L的两种一元碱MOH、ROH溶液中,PH随盐酸溶液体积的变化如图所示。下列说法正确的是
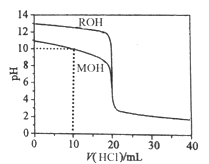
A. PH=10时,c(M+)>c(MOH)>c(Cl-)>c(OH-)>c(H+)
B. 将上述MOH、ROH溶液等体积混合后,用盐酸滴定至MOH恰好反应时:c(R+)>c(M+)>c(H+)>c(OH-)
C. 10mL<V(HCl)<20mL时,c(M+)+c(NOH)<c(Cl-)
D. V(HCl)>20mL时,不可能存在:c(Cl-)>c(M+)=c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向10 mL 0.1 mol·L-1 H2A溶液中滴加等浓度的NaOH溶液,溶液的pH与NaOH溶液的体积关系如图所示。下列叙述错误的是

A. C点溶液中含有NaHA和Na2A
B. NaHA溶液中水的电离程度比Na2A溶液中小
C. B点,c (Na+)=2[c (H2A)+c (HA)+c (A2-)]
D. D点,c (Na+)>c (A2-)>c (OH-)>c (HA-)>c (H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com