
| A. | 加入铝粉能产生H2的溶液中:K+、Mg2+、Cl-、SO42- | |
| B. | 加入Na2O2的溶液中:K+、Al3+、Cl-、NO3- | |
| C. | 含有0.1mol•L-1Ca2+的溶液中:Na+、K+、CO32-、Cl- | |
| D. | 无色透明的酸性溶液中:MnO4-、K+、SO42-、Na+ |
分析 A.加入铝粉能产生H2的溶液,为非氧化性酸或强碱溶液;
B.加入Na2O2的溶液,显碱性;
C.离子之间结合生成沉淀;
D.MnO4-为紫色.
解答 解:A.加入铝粉能产生H2的溶液,为非氧化性酸或强碱溶液,酸性溶液中该组离子之间不反应,可大量共存,故A选;
B.加入Na2O2的溶液,显碱性,不能大量存在Al3+,故B不选;
C.CO32-、Ca2+结合生成沉淀,不能共存,故C不选;
D.MnO4-为紫色,与无色不符,故D不选;
故选A.
点评 本题考查离子共存,为高频考点,把握习题中的信息及常见离子之间的反应是解本题关键,侧重分析与应用能力的考查,注意复分解反应的判断,题目难度不大.


科目:高中化学 来源: 题型:解答题
 “大象牙膏”的实验操作是向30%的过氧化氢溶液中加入少量二氧化锰和表面活性剂,现象如图.
“大象牙膏”的实验操作是向30%的过氧化氢溶液中加入少量二氧化锰和表面活性剂,现象如图.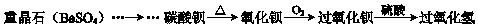
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCO3是弱电解质 | B. | CO2是弱电解质 | ||
| C. | 酸X一定是共价化合物 | D. | 酸X一定是强电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 50mL | B. | 60mL | C. | 70mL | D. | 80mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
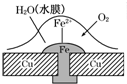 金属腐蚀是我们日常生活的常见现象.请根据如图回答下列问题:
金属腐蚀是我们日常生活的常见现象.请根据如图回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 50 | B. | 136 | C. | 86 | D. | 222 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com