
某溶液中由水电离出来的C(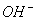 )=12-12mol/L,则该溶液中的溶质不可能是( )
)=12-12mol/L,则该溶液中的溶质不可能是( )
A.HCl B.NaOH C.NH4Cl D.H2SO4
科目:高中化学 来源: 题型:
下列各选项所述的两个量中,前者一定大于后者的是( )
A.纯水在100℃和25℃时pH
B.NH4Cl溶液中NH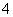 和Cl-的数目
和Cl-的数目
C.相同温度下,pH相同的NaOH溶液和Na2CO3溶液中由水电离出的c(OH-)
D.用0.1 mol/L的盐酸中和pH、体积均相同的氨水和NaOH溶液,所消耗盐酸的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
现有A、B、C、D、E、F六种化合物,已知它们的阳离子有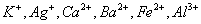 ,
, 阴离子有
阴离子有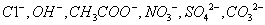 ,现将它们分别配成
,现将它们分别配成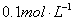 的溶液,进行如下实验:
的溶液,进行如下实验:
测得溶液A、C、E呈碱性,且碱性为A>E>C;
向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
向D溶液中滴加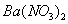 溶液,无明显现象;
溶液,无明显现象;
向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。
根据上述实验现象,回答下列问题:
实验②中反应的化学方程式是
;
(2)E溶液是 ,判断依据是
;
(3)写出下列四种化合物的化学式:A 、C 、
D 、F .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列浓度关系正确的是
A. 氯水中:c(Cl2)=2[c(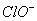 )+c(
)+c(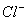 )+C(HClO)]
)+C(HClO)]
B. 氯水中:c(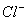 )>c(
)>c(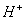 )>c(
)>c(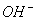 )>c(
)>c(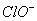 )
)
C. 等体积等浓度的氢氧化钠与醋酸混合:c(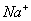 )=c(
)=c(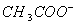 )
)
D. 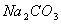 溶液中:c
溶液中:c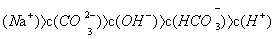
查看答案和解析>>
科目:高中化学 来源: 题型:
难溶化合物的饱和溶液存在着溶解平衡,例如:
AgCl(s) 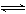 Ag++
Ag++ ,Ag2CrO4(s)
,Ag2CrO4(s) 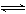 2Ag++
2Ag++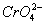 ,在一定温度下,难溶化合物饱和溶液离子浓度的乘积为一常数,这个常数用Ksp表示。
,在一定温度下,难溶化合物饱和溶液离子浓度的乘积为一常数,这个常数用Ksp表示。
已知:Ksp(AgCl)=[Ag+][ ]=1.8×12-12
]=1.8×12-12
Ksp(Ag2CrO4)=[Ag+]2[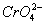 ]=1.9×12-12
]=1.9×12-12
现有0.001摩/升AgNO3溶液滴定0.001摩/升KCl和0.001摩/升的K2CrO4的混和溶液,试通过计算回答:
(1)  和
和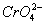 中哪种先沉淀?
中哪种先沉淀?
(2)当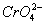 -以Ag2CrO4形式沉淀时,溶液中的
-以Ag2CrO4形式沉淀时,溶液中的 Cl-离子浓度是多少?
Cl-离子浓度是多少? 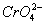 与
与 能否达到有效的分离?(设当一种离子开始沉淀时,另一种离子浓度小于12-5mol/L时,则认为可以达到有效分离)
能否达到有效的分离?(设当一种离子开始沉淀时,另一种离子浓度小于12-5mol/L时,则认为可以达到有效分离)
查看答案和解析>>
科目:高中化学 来源: 题型:
欲使NaHCO3溶液中的c(H+)、c(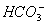 )、c(
)、c(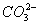 )都减少,其方法是 ( )
)都减少,其方法是 ( )
A.通入CO2气体 B.通入HCl气体
C.加入NaOH固体 D.加入Ca(OH)2固体
查看答案和解析>>
科目:高中化学 来源: 题型:
现有浓度均为0.1 mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵,⑧氨水,请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号) 。
(2)④、⑤、⑥、⑦、⑧五种溶液中NH4+浓度由大到小的顺序是(填序号) 。
(3)将③和④等体积混合后,混合液中各离子浓度由大到小的顺序是 。
(4)已知t℃,KW=1×12-13,则t℃(填“>”或“<”或“=”) 25℃。在t℃时将pH=11的NaOH溶液a L与pH=1的H2SO4的溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a∶b= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ。且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H-O键形成时放出热量463 kJ,则氢气中1mol H-H键断裂时吸收热量为( )
A.920 kJ B.557 kJ C.436 kJ D.188 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com