
| A. | 用小苏打作发酵粉焙制糕点 | B. | 用甲醛溶液浸泡海产品 | ||
| C. | 用工业石蜡给水果上蜡“美容” | D. | 用工业酒精勾兑饮用酒 |
分析 A、根据碳酸氢钠的化学性质判断.
B、根据甲醛的毒性判断.
C、根据工业石蜡含有有害物质判断.
D、根据工业酒精的成分和甲醇的毒性判断.
解答 解:A、碳酸氢钠能与面粉发酵产生的酸反应生成二氧化碳气体,也能受热分解产生二氧化碳气体,使食品疏松多孔,所以A正确.
B、甲醛有毒,能破坏人体蛋白质的结构,使之失去生理功能,所以B错误.
C、工业石蜡含有有害物质,不能食用,所以C错误.
D、工业酒精的成分中含有甲醇,甲醇有毒,不能饮用,所以D错误.
故选A.
点评 食品安全是当今社会关注的重要热点之一,与食品加工相关的化学物质或添加剂的知识考查也越来越突显出来,特别是关于发酵粉、甲醛、工业酒精、亚硝酸盐、食用石蜡等物质的使用,以及农药化肥不合理施用,化学元素添加过量等带来的食品安全问题,在考查中出现的频度越来越高.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ④ | C. | ②③ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L盐酸和0.1mol/L醋酸分别与0.2mol/L氢氧化钠溶液反应的速率相同 | |
| B. | 0.1mol/L盐酸和0.1mol/L硝酸分别与大小相同的大理石反应的速率相同 | |
| C. | 铝和铁分别与0.1mol/L硫酸的反应速率相同 | |
| D. | 大理石块与大理石粉末分别与0.1mol/L盐酸反应的速率相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
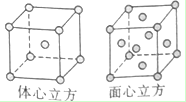 X、Y、Z、W为前四周期元素且原子序数依次增大,X的电子层数等于核外电子数,Y元素基态原子核外未成对电子数为2且X与Y形成的化合物在常温下为常见的液体R,Z元素原子最外电子层上s、p电子数相等,W基态原子3d轨道的电子数是4s轨道电子数的3倍.请回答下列问题:
X、Y、Z、W为前四周期元素且原子序数依次增大,X的电子层数等于核外电子数,Y元素基态原子核外未成对电子数为2且X与Y形成的化合物在常温下为常见的液体R,Z元素原子最外电子层上s、p电子数相等,W基态原子3d轨道的电子数是4s轨道电子数的3倍.请回答下列问题: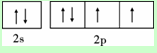 ,其第一电离能在同周期元素中由大到小排第4 位.
,其第一电离能在同周期元素中由大到小排第4 位.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制CuSO4时先将Cu氧化成CuO后再与稀硫酸反应 | |
| B. | 采用银作催化剂,乙烯和氧气制取环氧乙烷,原子利用率100% | |
| C. | 用乙醇代替汽油作汽车燃料 | |
| D. | 用稀硝酸和铜制取Cu(NO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 价层电子对互斥理论将分子分成两类:中心原子有孤电子对的和无孤电子对的 | |
| B. | 价层电子对互斥理论既适用于单质分子,也适用于化合物分子 | |
| C. | sp3杂化轨道是由一个原子中能量相近的s轨道和p轨道通过杂化形成的一组能量相近的新轨道 | |
| D. | AB2型共价化合物的中心原子A采取的杂化方式可能不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
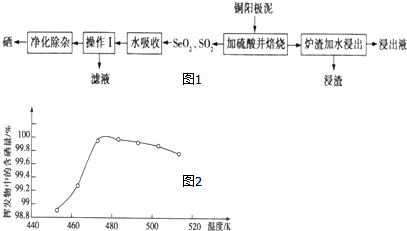
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com