
下列各组溶液中,c (Cl-) 最大的是
A.500 mL 1 mol/L KCl B.800 mL 0.5 mol/L MgCl2
C.250 mL 1 mol/L FeCl3 D.200 mL 1 mol/L CaCl2
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
短周期元素离子aA2+、bB+、cC3-、dD-都具有相
同电子层结构,则下列叙述正确的是( )
A.原子半径A>B>D>CB.原子序数d>c>b>a
C.离子半径C>D>B>AD.单质还原性A>B>D>C
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的化学名称、化学式和俗名一致的是( )
A.碳酸钙、CaCO3、生石灰 B.氢氧化钠、NaOH、纯碱
C.碳酸钠、Na2CO3、苏打 D.碳酸氢钠、NaHCO3、苏打
查看答案和解析>>
科目:高中化学 来源: 题型:
小明体检的血液化验单中,葡萄糖为5.9×10-3mol/L。表示该体检指标的物理量是
A.溶解度(s) B.物质的量浓度(c) C.质量分数(w) D.摩尔质量(M)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学反应方程式中,不能用离子方程式Ba2++SO42-=BaSO4↓ 表示的是
A.Ba(NO3)2 + H2SO4 = BaSO4↓ + 2HNO3
B.BaCl2 + Na2SO4 = BaSO4↓ + 2NaCl
C.BaCO3 + H2SO4 = BaSO4↓ + H2O + CO2↑
D.BaCl2 + H2SO4 = BaSO4↓ + 2HCl
查看答案和解析>>
科目:高中化学 来源: 题型:

 现有下列物质:①Na2CO3•10H2O晶体 ②锌 ③氯化氢 ④CO2 ⑤NaHSO4固体 ⑥Ba(OH)2 固体 ⑦红褐色的氢氧化铁液体 ⑧氨水 ⑨稀硫酸 ⑩熔融NaCl ⑾ 蔗糖 (1)按物质的分类方法填写表格的空白处 (填编号) :
现有下列物质:①Na2CO3•10H2O晶体 ②锌 ③氯化氢 ④CO2 ⑤NaHSO4固体 ⑥Ba(OH)2 固体 ⑦红褐色的氢氧化铁液体 ⑧氨水 ⑨稀硫酸 ⑩熔融NaCl ⑾ 蔗糖 (1)按物质的分类方法填写表格的空白处 (填编号) :
| 分类标准 | 能导电的物质 | 电解质 | 非电解质 |
| 属于该类的物质 |
|
 (2)上述物质中有物质之间在溶液中可发生离子反应:H++OH-══H2O,写出一个该离子反应对应的化学方程式
(2)上述物质中有物质之间在溶液中可发生离子反应:H++OH-══H2O,写出一个该离子反应对应的化学方程式
(3)将⑨滴加到⑦中至过量的实验现象是
(4)将③通入⑧中至恰好完全反应,则溶液导电能力的变化为
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各化学反应的离子方程式中,有错误的是( )
A.铝与氢氧化钠反应:2Al+2OH-+2H2O=2AlO2-+3 H2↑
B.氧化铝溶于氢氧化钠溶液:Al2O3+2OH-=2AlO2-+H2O
C.碘化亚铁溶液中滴入足量溴水:2Fe2++2I-+2Br2=I2+2Fe3++4Br-
D.碳酸氢镁溶液中加过量澄清石灰水
Mg2++2HCO3-+2Ca2++4OH-=2CaCO3↓+2H2O+Mg(OH)2↓
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。
完成下列填空,
(1)Se和浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1:1,写出Se和浓HNO3的反应方程式 。
如不对该反应还原产物的比例作限制,该反应 出现多组配平系数(填“可能”或“不可能”)并说明理由 。
(2)回收得到的SeO2的含量,可以通过下面的方法测定:
①SeO2+KI十HNO3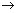 Se+I2+KNO3十H2O
Se+I2+KNO3十H2O
②I2+2Na2S2O3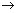 Na2S4O6+2NaI
Na2S4O6+2NaI
实验中,准确称量SeO2样品0.160 0 g,消耗了0.200 0 mol L-1的Na2S2O3溶液25.00mL,所测定的样品中SeO2的质量分数为
L-1的Na2S2O3溶液25.00mL,所测定的样品中SeO2的质量分数为
Ⅱ.高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝、助凝、杀菌、除臭为一体的新型高效多功能绿色水处理剂,具有良好的应用前景。其生产工艺如下:
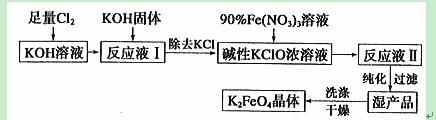
已知:①2KOH+Cl2 KCl+KClO+H2O(条件:温度较低)
KCl+KClO+H2O(条件:温度较低)
②6KOH+3C12 5KCl+KClO3+3H2O(条件:温度较高)
5KCl+KClO3+3H2O(条件:温度较高)
回答下列问题:
(1)该生产工艺应在 (填“温度较高’’或“温度较低”)的情况下进行。
(2)写出Fe(NO3)3在强碱性条件下与KClO反应制K2FeO4的离子方程式 。
(3)在“反应液Ⅰ”中加KOH固体的目的是 (填序号)。
A.与“反应液Ⅰ”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3化为KClO
查看答案和解析>>
科目:高中化学 来源: 题型:
雾霾严重影响人们的生活与健康。某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl- 。某同学收集了该地区的雾霾,经必要的预处理后得试样溶液,设计并完成了如下的实验:
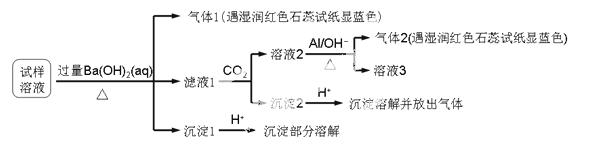
已知:3NO3- + 8Al + 5OH- + 2H2O 
 3NH3 + 8AlO2-
3NH3 + 8AlO2-
根据以上的实验操作与现象,该同学得出的结论不正确的是
A.试样中肯定存在NH4+、Mg2+、SO42-和NO3-
B.试样中一定不含Al3+
C.试样中可能存在Na+、Cl -
-
D.该雾霾中可能存在NaNO3 、NH4Cl和MgSO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com