
【题目】足量的镁条分别在体积相同的①O2、②N2、③CO2中充分燃烧,所得固体的质量由大到小的正确顺序是( )
A. ①②③ B. ③②① C. ②①③ D. ②③①
科目:高中化学 来源: 题型:
【题目】室温下某溶液中由水电离出的H+浓度为1.0×10﹣13molL﹣1,则在此溶液中一定不可能大量存在的离子组是( )
A. Al3+、K+、NO3﹣、Cl﹣ B. K+、Na+、HCO3﹣、Cl﹣
C. Na+、CO32﹣、SO42﹣、NO3﹣ D. Ba2+、Na+、Cl﹣、NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】传统医学治疗疟疾时将青蒿加水煮沸,但药效很差。改用乙醇控温60℃提取青蒿素,药效显著提高。屠呦呦用一种更适宜的物质从青蒿中提取青蒿素,这种提取物对疟原虫的抑制率达到了100%,这种适宜的物质是
A | B | C | D | |
物质 | 乙醚 | 四氯化碳 | 丙醇 | 煤油 |
沸点℃ | 34.5 | 76.5 | 97.4 | 180-310 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填写下列空白:
(1)有6.02×l023个H的H2O,其物质的量是_______;1molNa2SO4中所含的离子总数目为______。
(2)_____molH2O中含有的氧原子数与1.5molCO2中含有的氧原子数相等。
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为_______。
(4)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为________。
(5)标准状况下,密度为0.75g·L-1的NH3与CH4组成的混合气体中,该混合气体对氢气的相对密度为____________。
(6)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨基甲酸铵(H2NCOONH4)是一种易分解、易水解的白色固体,某研究小组用下图所示的实验装置,利用氢氧化钠固体、浓氨水、干冰等作原料制备氨基甲酸铵。主要反应原理:2NH3(g) + CO2(g)=H2NCOONH4(s) ΔH<0。
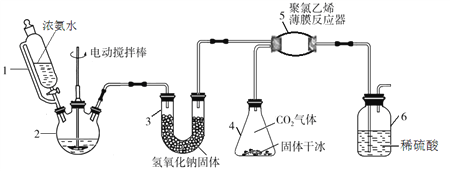
(1)仪器2的名称是_____________。仪器3中NaOH固体的作用是_____________。
(2)仪器6的一个作用是控制原料气按反应计量系数充分反应,若反应初期观察到装置内稀硫酸溶液中产生气泡,应该_____________(填“加快”、“减慢”或“不改变”)产生氨气的流速。
(3)另有一种制备氨基甲酸铵的反应器(CCl4充当惰性介质)如下图:
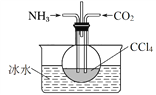
①若无冰水,则氨基甲酸铵易分解生成尿素[化学式为CO(NH2)2]。请写出氨基甲酸铵受热分解的化学反应方程式:_____________。
②当CCl4液体中产生较多晶体悬浮物时,即停止反 应,过滤分离得到粗产品,为了将所得粗产品干燥可采取的方法是_____________。
A.蒸馏 B.高压加热烘干 C.真空微热烘干
(4)已知氨基甲酸铵可完全水解为碳酸氢铵,则该反应的化学方程式为_____________。
为测定某样品中氨基甲酸铵的质量分数,某研究小组用该样品进行实验。已知杂质不参与反应,请补充完整测定某样品中氨基甲酸铵质量分数的实验方案:用天平称取一定质量的样品,加水溶解,_____________,测量的数据取平均值进行计算(限选试剂:蒸馏水、澄清石灰水、BaCl2溶液)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为Pb+PbO2+4H++2SO![]()
![]() 2PbSO4+2H2O,则下列说法正确的是( )
2PbSO4+2H2O,则下列说法正确的是( )
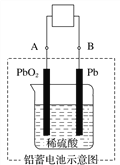
A. 放电时:电子流动方向由A经导线流向B
B. 放电时:正极反应是Pb-2e-+SO![]() ===PbSO4
===PbSO4
C. 充电时:铅蓄电池的负极应与充电器的正极相连
D. 充电时:阳极反应是PbSO4-2e-+2H2O===PbO2+SO![]() +4H+
+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H3BO3可以通过电解NaB(OH)4溶液的方法制备,其工作原理如图,下列叙述错误的是
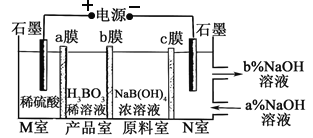
A. M室发生的电极反应式为:2H2O-4e- = O2↑+4H+
B. N室中:a% <b%
C. b膜为阴离子交换膜
D. 理论上每生成1mol产品,阴极室可生成5.6L气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2S(g)+O2(g)===S2(s)+2H2O(l) ΔH=-632 kJ·mol-1。右图为H2S燃料电池的示意图。下列说法正确的是( )
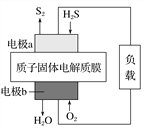
A. 电极a为电池的正极
B. 电极b上发生的电极反应为O2+2H2O+4e-===4OH-
C. 每有1 mol氧气参加反应,电池内部吸收632 kJ热能
D. 每34 g H2S参与反应,电路中有2 mol电子通过
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示实验装置,烧瓶内充满氯气,底部有一层细沙(不参与反应),玻璃导管下口b处塞有一小块钠。从a口伸入一根细铁丝把钠块捅下去,再用滴管从a口滴下一滴水,恰好落在钠块上,立即剧烈反应。下列对此实验的说法中,不正确的是()
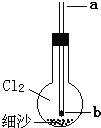
A. 所充氯气应用向上排空气法收集
B. 反应中,烧瓶内产生大量白色烟雾
C. 玻璃导管只起到定位加入钠和水的作用
D. 烧瓶中Cl2,可能参与四个氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com