

科目:高中化学 来源:不详 题型:单选题
| A.少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 |
| B.当出现CO中毒时,应立即将中毒者抬到室外新鲜空气处 |
| C.制取并排水法收集氧气结束后,应立即停止加热 |
| D.将含硫酸的废液倒入水槽,用水冲人下水道 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 |
| B.不慎将浓碱溶液沾到皮肤上,要立即用大量的水冲洗,然后涂上硼酸溶液 |
| C.金属钠着火,应立即用沙子灭火 |
| D.配制浓硫酸时,可先在量筒中加一定体积的水,再在搅拌下慢慢加入浓硫酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

| A.KMnO4溶液 | B.Fe粉 | C.Na2CO3溶液 | D.KSCN溶液 |
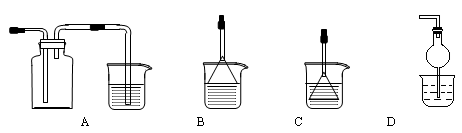
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
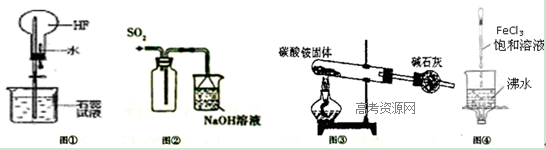
| A.利用图①装置做喷泉实验 |
| B.利用图②装置收集SO2并吸收尾气 |
| C.实验室里利用图③装置制取少量纯净的氨气 |
| D.利用图④装置制备氢氧化铁胶体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.预测物质的性质 | B.观察物质的外观状态 |
| C.进行实验和观察 | D.作出相关的解释和结论 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.存放新制氯水时,使用带玻璃塞的棕色玻璃瓶 |
| B.配制一定物质的量浓度的溶液时,若开始容量瓶中有少量蒸馏水,对浓度无影响 |
| C.酸碱中和滴定实验中用到的玻璃仪器仅有酸式滴定管、碱式滴定管和烧杯 |
| D.进行蒸发操作时,不能使混合物中的水分完全蒸干 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com