
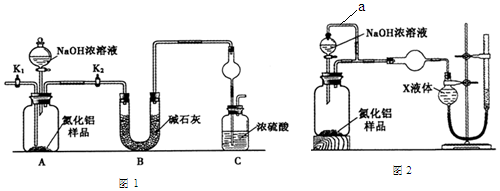
分析 (1)氨气是和浓硫酸能发生反应的气体,易发生倒吸;
(2)组装好实验装置,依据原理可知气体制备需要先检查装置气密性,加入实验药品.接下来的实验操作是关闭K1,打开K2,反应生成氨气后卫把装置中的气体全部赶入装置C被浓硫酸吸收,准确测定装置C的增重计算;
(3)装置存在缺陷是空气中的水蒸气和二氧化碳也可以进入装置C,使测定结果偏高,需要连接一个盛碱石灰干燥管;
(4)导管a保持恒压便于液体流下,减少测定气体体积的误差;
(5)氨气极易溶于水,量气装置中的X液体不能与氨气反应,不能使氨气溶解;
(6)依据AIN+NaOH+H2O═NaAIO2+NH3↑在定量关系计算.
解答 解:(1)氨气是与浓硫酸能发生反应的气体,易发生倒吸,图C装置中球形干燥管的作用是防止倒吸的作用,
故答案为:防止倒吸;
(2)组装好实验装置,需要先检查装置气密性,加入实验药品.接下来的实验操作是关闭K1,打开K2,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体.打开K1,通入氮气一段时间,测定C装置反应前后的质量变化.通入氮气的目的是,反应生成氨气后卫把装置中的气体全部赶入装置C被浓硫酸吸收,准确测定装置C的增重计算,
故答案为:检查装置气密性;关闭K1,打开K2;把装置中残留的氨气全部赶入C装置;
(3)装置存在缺陷是空气中的水蒸气和二氧化碳也可以进入装置C,使测定结果偏高,需要连接一个盛碱石灰干燥管,
故答案为:C装置出口处连接一个干燥装置;
(4)导管a的主要作用是:保持气压恒定,使NaOH浓溶液容易流下,
故答案为:保持气压恒定,使NaOH浓溶液容易流下;
(5)a.CCl4不能溶解氨气,可以用排四氯化碳溶液的方法测定氨气体积,故a正确;
b.氨气极易溶于水,不能排水法测定,故b错误;
c.氨气极易溶于水,不能用排NH4Cl溶液的方法测定气体体积,故c错误;
d.氨气不溶于苯,可以利用排苯溶液,测定氨气的体积,故d正确;
故答案为:ad;
(6)若m g样品完全反应,测得生成气体的体积为V mL(已转换为标准状况),
AlN+NaOH+H2O═NaAIO2+NH3↑
41 22.4L
m V×10-3L
m=$\frac{41V×1{0}^{-3}}{22.4}$g,
则AlN的质量分数=$\frac{41V×1{0}^{-3}}{22.4m}$×100%=$\frac{41V}{22400m}$×100%,
故答案为:$\frac{41V}{22400m}$×100%.
点评 本题考查了物质含量的测定探究实验设计和实验分析判断,把握实验基本操作和物质性质是解题关键,题目难度中等,注意把握实验原理以及各部操作的目的,侧重于考查学生的实验能力和计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑ | |
| B. | 向稀硝酸中滴加Na2SO3溶液:SO32-+2H+=SO2↑+H2O | |
| C. | 向Al2(SO4)3溶液中加入过量NH3•H2O:Al3++4NH3•H2O=[AI(OH)4]-+4NH4+ | |
| D. | 向Na2SiO3溶液中通入过量SO2:SiO32-+SO2+H2O=H2SiO3↓+SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
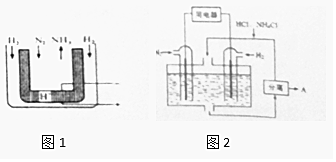 氮及其化合物与人类的生产、生活息息相关.
氮及其化合物与人类的生产、生活息息相关.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | C-C | C-H | H-H | C-O | C≡O | O-H |
| 键能/kJ•mol-1 | 348 | 413 | 436 | 358 | x | 463 |
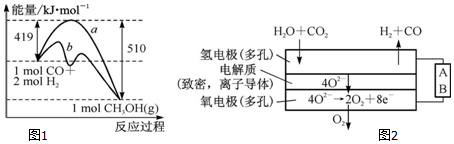
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/mol•L-1 | 0.5 | 2 | 2 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
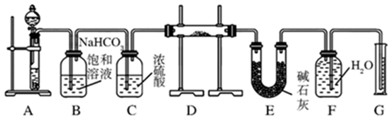
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
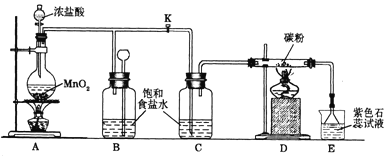
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com