
【题目】碲(Te)具有两性特征,铜阳极泥是提取碲的主要原料,碲在铜阳极泥中主要以MezTeCMe表 示金属Cu、Pb、Au、Ag等)的形式存在。
(1)利用“氯化浸出-还原法”制备Te的工艺流程如下所示。
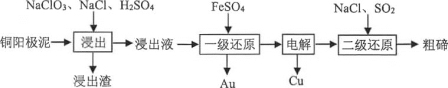
①浸出液的主要成分为CuSO4、HAuCu、H2TeO3,则浸出渣的主要成分 为____(填化学式);“浸出”过程中有少量污染性气体生成,该气体是_______(填物质名称)
②已知HAuCU是一种强酸,则“一级还原”过程中发生反应的离子方程式为_________。
③欲得到64g碲,则“二级还原”过程中至少需通入____mol SO2。 “氧化碱浸-电解法”指的是在氧化剂的作用下,Cu2Te与NaOH溶液反应生成Na2TeO3和Cu(OH)2,经电解即可获得Te。
①以空气为氧化剂进行“氧化碱浸”的化学方程式为______。
②电解过程中,阴极的电极反应式为______。
③与“氯化浸出-还原法”相比“氧化碱浸-电解法”的优点是____(任写一点)
【答案】PbSO4和AgCl 氯气 [AuCl4]- + 3Fe2+ = 3Fe3+ + Au + 4Cl- 1 Cu2Te + 2O2 + 2NaOH + H2O = Na2TeO3 + 2Cu(OH)2 TeO32- + 4e- + 3H2O = Te + 6OH- 不生成氯气等污染性气体(或工艺简单)
【解析】
(1)①Pb和Ag被氧化成Pb2+和Ag+,随后分别与SO42-和Cl-形成沉淀PbSO4和AgCl,浸出渣的主要成分为PbSO4和AgCl。NaCl中Cl-与溶液中的氧化得到的少量Au3+络合,形成四氯合金离子([AuCl4]-),促进Au的溶解,同时使Ag+沉淀。NaClO3和NaCl反应生成氯气Cl2,故“浸出”过程中需要进行尾气处理的污染性气体是Cl2。
②“一级还原”过程中发生反应的离子方程式为:[AuCl4]-+3Fe2+=3Fe3++Au↓+4Cl-;
③H2TeO3→Te,Te元素化合价变了4价,SO2→SO42-,硫元素化合价变了2价,根据得失电子守恒有0.5mol×4=n(SO2)×2(其中64g的碲为0.5mol),解得n(SO2)=1mol。
(2)①在氧化剂的作用下,Cu2Te与NaOH溶液反应生成Na2TeO3,化学方程式为Cu2Te+2O2+2NaOH+H2O=Na2TeO3+2Cu(OH)2。
②若用惰性电极电解溶液,在阴极上TeO32-得到电子生成Te,电极反应式为TeO32-+4e-+3H2O=Te+6OH-。
③与“氯化浸出-还原法”相比,“氧化碱浸-电解法”的优点是如不产生氯气等污染性气体,反应步骤少,简便,成本低等。
(1)①Pb和Ag被氧化成Pb2+和Ag+,随后分别与SO42-和Cl-形成沉淀PbSO4和AgCl,浸出渣的主要成分为PbSO4和AgCl。NaCl中Cl-与溶液中的氧化得到的少量Au3+络合,形成四氯合金离子([AuCl4]-),促进Au的溶解,同时使Ag+沉淀。NaClO3和NaCl反应生成氯气Cl2,故“浸出”过程中需要进行尾气处理的污染性气体是Cl2。
②“一级还原”过程中发生反应的离子方程式为:[AuCl4]-+3Fe2+=3Fe3++Au↓+4Cl-;
③H2TeO3→Te,Te元素化合价变了4价,SO2→SO42-,硫元素化合价变了2价,根据得失电子守恒有0.5mol×4=n(SO2)×2(其中64g的碲为0.5mol),解得n(SO2)=1mol。
(2)①在氧化剂的作用下,Cu2Te与NaOH溶液反应生成Na2TeO3,化学方程式为Cu2Te+2O2+2NaOH+H2O=Na2TeO3+2Cu(OH)2。
②若用惰性电极电解溶液,在阴极上TeO32-得到电子生成Te,电极反应式为TeO32-+4e-+3H2O=Te+6OH-。
③根据以上分析可知与“氯化浸出-还原法”相比“氧化碱浸-电解法”的优点是如不产生氯气等污染性气体,反应步骤少,简便,成本低等。


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:
【题目】过氧化钠与水反应后滴加酚酞,酚酞先变红后褪色。某小组欲探究其原因,进行以下实验:①取反应后溶液加入二氧化锰后迅速产生大量气体;实验②、③中红色均不褪去。下列分析错误的是

A. 过氧化钠与水反应产生的气体为O2
B. 过氧化钠与水反应需要MnO2作催化剂
C. 实验②、③证明使酚酞褪色的不是氢氧化钠和氧气
D. 过氧化钠与水反应可能生成了具有漂白性的H2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷在加热条件下可还原氧化铜,气体产物除水蒸气外,还有碳的氧化物。某化学小组利用如图装置探究其反应产物。
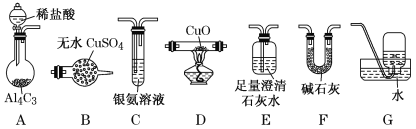
[查阅资料]①CO能与银氨溶液反应:CO+2[Ag(NH3)2]++2OH-=2Ag↓+2NH4++CO32-+2NH3。
②Cu2O为红色,不与Ag+反应,能发生反应:Cu2O+2H+=Cu2++Cu+H2O。
(1)装置A中反应的化学方程式为___。
(2)按气流方向各装置从左到右的连接顺序为A→__。(填字母编号)
(3)已知气体产物中含有CO,则装置C中可观察到的现象是___装置F的作用为__。
(4)当反应结束后,装置D处试管中固体全部变为红色。设计实验证明红色固体中含有Cu2O:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把镁条投入盛有盐酸的敞口容器中,产生氢气的速率变化曲线如图所示。下列因素中,影响该反应速率的主要因素是

①盐酸的浓度 ②镁条的表面积 ③溶液的温度 ④Cl-的浓度
A. ①④ B. ③④ C. ①③ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示是以海水为原料,获得某产物的工艺流程图。已知在吸收塔中,溶液的pH显著减小。试回答下列问题:

(1)图中两次氯化的作用是否相同________(选填“是”或“否”)。
(2)吸收塔中反应的化学方程式为_______________________________,第2次氯化的离子方程式为_________________________________________________。
(3)资料证实,在酸性介质中,第1次氯化过程中可用氧气或空气替代。但在实际工业生产中为什么不用更廉价的空气替代氯气________________________。
(4)本工艺的处理方法可简单概括为“空气吹出、X气体吸收、氯化”。某同学认为在工业生产过程中对第1次氯化液直接蒸馏也可得到产物,不必进行上述过程,请对该同学的说法作出正确的评价___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示甲是某学生验证铜和浓硝酸反应的装置,乙、丙是另外两位同学对甲装置改进后的装置:
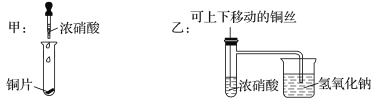
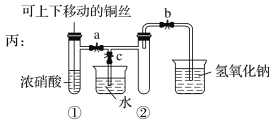
(1)甲、乙、丙三个装置中共同发生的反应的化学方程式是__________________________________。
(2)和甲装置相比,乙装置的优点是①______________________;②________________。
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置。实验时先关闭活塞________,再打开活塞________,才能使NO2气体充满②试管;当气体充满②试管后,将铜丝提起与溶液脱离。欲使烧杯中的水进入②试管,应该_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钯的化合物氯化钯可用来检测有毒气体CO,发生反应的化学方程式为:![]() 。下列说法正确的是()
。下列说法正确的是()
A.题述反应条件下还原性:CO>Pd
B.题述反应中PdCl2被氧化
C.生成22.4 L CO2时,转移的电子为2 mo1
D.CO气体只有在高温下才能表现还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】病人输液用的葡萄糖注射液是葡萄糖(化学式为C6H12O6)的水溶液,其标签上的部分内容如图所示。利用标签所提供的信息,回答下列问题:

(1)该注射液中葡萄糖的质量分数为__________(该溶液密度约为 1.0 g/cm3)。
(2)该注射液中葡萄糖的物质的量浓度是__________mol/L(计算结果精确到小数点后2位)。
(3)某同学进行某项实验需要480 mL上述葡萄糖溶液,其配制过程如下,请完成填空:
①该同学需称取________g葡萄糖在烧杯中溶解;
②配制时,正确的操作顺序是(用字母表示,每个字母只能用一次)________;
A.用50 mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用托盘天平准确称取葡萄糖并加入盛有少量水(约50 mL)的烧杯中,用玻璃棒慢慢搅拌,使其完全溶解
C.将已溶解完全的葡萄糖溶液沿玻璃棒注入一定规格的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹液面的最底处恰好与刻度线相切
F.继续往容量瓶内小心加水,至液面离容量瓶颈刻度线下1~2 cm 处
③在配制过程中,下列实验操作使所配制的葡萄糖溶液的物质的量浓度偏高的是________(填字母代号);
A.用托盘天平称取葡萄糖时“左物右码”
B.溶解时使用的烧杯和玻璃棒未洗涤
C.洗净的容量瓶未经干燥就用于配制溶液
D.定容时俯视凹液面
E.加水超过刻度线后,用胶头滴管吸出多余的液体
(4)已知溶液中某溶质的物质的量除以溶剂的质量称为该溶质的质量摩尔浓度,单位为mol/kg。
①上述葡萄糖溶液的质量摩尔浓度为________(计算结果精确到小数点后2位)mol/kg。
②若将标准状况下a L HCl气体完全溶于b g水中,此时该盐酸的质量摩尔浓度为______(只需列出计算式,无需化简)mol/kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有抗菌作用的白头翁素衍生物H的合成路线如下图所示:
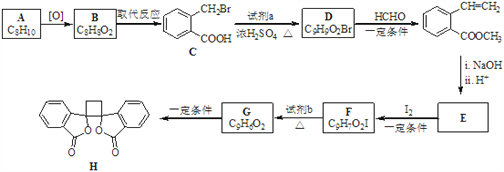
已知:i.RCH2Br ![]() R﹣HC═CH﹣R′
R﹣HC═CH﹣R′
ii.R﹣HC═CH﹣R′![]()
![]()
iii.R﹣HC═CH﹣R′![]()
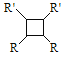
(以上R、R'、R'代表氢、烷基或芳基等)
(1)A属于芳香烃,其名称是_______________________。
(2)D的结构简式是_______________________________。
(3)由F生成G的反应类型是________________________________________。
(4)由E与I2在一定条件下反应生成F的化学方程式是_____________________;此反应同时生成另外一个有机副产物且与F互为同分异构体,此有机副产物的结构简式是_______________________________。
(5)下列说法正确的是___________(选填字母序号)。
A. G存在顺反异构体
B. 由G生成H的反应是加成反应
C. 1 mol G最多可以与1 mol H2发生加成反应
D. 1 mol F或1 mol H与足量NaOH溶液反应,均消耗2 molNaOH
(6)以乙烯为起始原料,结合已知信息选用必要的无机试剂合成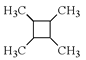 写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。___________________
写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。___________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com