
·ÖĪö ĖÄĀČ»ÆĢ¼”¢±½¶¼²»ČÜÓŚĖ®£¬ĖÄĀČ»ÆĢ¼µÄĆܶȱČĖ®“󣬱½µÄĆܶȱČĖ®Š”£¬ŅŅĻ©ŗ¬ÓŠĢ¼Ģ¼Ė«¼ü£¬Óėäå·¢Éś¼Ó³É·“Ó¦£¬ŅŅ“¼ÓėĖ®»ģČÜ£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗ£Ø1£©ĖÄĀČ»ÆĢ¼”¢±½¶¼²»ČÜÓŚĖ®£¬¼ÓČėäåĖ®£¬ČÜŅŗ·Ö²ć£¬¹Ź“š°øĪŖ£ŗAC£»
£Ø2£©äåŅ×ČÜÓŚ±½”¢ĖÄĀČ»ÆĢ¼£¬ÓŠ»ś²ćŃÕÉ«ÓÉĪŽÉ«±äÉ«³ČÉ«£¬Ė®²ćĪŽÉ«£¬ŅŅĻ©ÓėäåĖ®·“Ó¦¶ųŹ¹äåĖ®ĶŹÉ«£¬¹Ź“š°øĪŖ£ŗABC£»
£Ø3£©±½µÄĆܶȱČĖ®Š”£¬¼ÓČėäåĖ®£¬äåŅ×ČÜÓŚ±½£¬ĻĀ²ćĪŖĖ®£¬ŃÕÉ«ĪŖĪŽÉ«£¬¹Ź“š°øĪŖ£ŗC£»
£Ø4£©ŅŅĻ©ŗ¬ÓŠĢ¼Ģ¼Ė«¼ü£¬æÉÓėäå·¢Éś¼Ó³É·“Ó¦£¬¹Ź“š°øĪŖ£ŗB£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄ¼ų±š£¬ĢāÄæÄŃ¶Č²»“󣬱¾Ģā×¢Ņā°ŃĪÕÓŠ»śĪļµÄŠŌÖŹµÄŅģĶ¬£¬×¢Ņā³£¼ūÓŠ»śĪļµÄĪļĄķŠŌÖŹ£¬ŌŚŃ§Ļ°ÖŠ³£³£æ¼²é£¬²»ÄÜŗöŹÓ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŹĒ×ī¼ņµ„µÄÓŠ»ś»ÆŗĻĪļ | |
| B£® | ŌŚ1500”ęŅŌÉĻÄÜ±Č½ĻĶźČ«µŲ·Ö½ā£¬Éś³ÉĢæŗŚŗĶĒāĘų | |
| C£® | ÓėµČĪļÖŹµÄĮæµÄĀČĘų»ģŗĻŌŚ¹āÕÕĻĀ³ä·Ö·“Ó¦£¬Éś³ÉĪļÖŠHC1µÄĪļÖŹµÄĮæ×ī“ó | |
| D£® | ĶźČ«Č¼ÉÕÉś³ÉµÄCO2ŗĶH2OµÄĪļÖŹµÄĮæÖ®±ČŹĒ1£ŗ1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
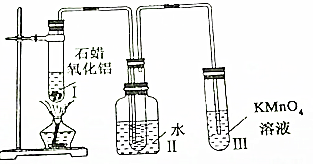
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
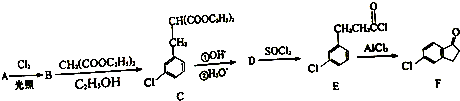
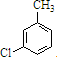 £¬·“Ó¦D”śEµÄ·“Ó¦ĄąŠĶČ”“ś·“Ó¦£®
£¬·“Ó¦D”śEµÄ·“Ó¦ĄąŠĶČ”“ś·“Ó¦£®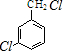 +Cl2$\stackrel{¹āÕÕ}{”ś}$
+Cl2$\stackrel{¹āÕÕ}{”ś}$ +HCl£®
+HCl£®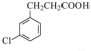 £¬Ä³»ÆѧĪļŹĒDµÄĶ¬·ÖŅģ¹¹Ģ壬ÄÜŹ¹FeCl3ČÜŅŗĻŌ×ĻÉ«£¬ĒŅ·Ö×ÓÖŠÖ»ÓŠ3ÖÖ²»Ķ¬»Æѧ»·¾³µÄĒā£¬Š“³öøĆ»ÆŗĻĪļµÄ½į¹¹¼ņŹ½£ŗ
£¬Ä³»ÆѧĪļŹĒDµÄĶ¬·ÖŅģ¹¹Ģ壬ÄÜŹ¹FeCl3ČÜŅŗĻŌ×ĻÉ«£¬ĒŅ·Ö×ÓÖŠÖ»ÓŠ3ÖÖ²»Ķ¬»Æѧ»·¾³µÄĒā£¬Š“³öøĆ»ÆŗĻĪļµÄ½į¹¹¼ņŹ½£ŗ »ņ
»ņ £ØČĪŠ“Ņ»ÖÖ£©£®
£ØČĪŠ“Ņ»ÖÖ£©£® £®
£®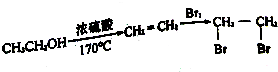
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ēč·Ö×ÓÖŠĖÄŌ×Ó¹²Ö±Ļߣ¬ŹĒŗ¬ÓŠ¼«ŠŌ¼üµÄ·Ē¼«ŠŌ·Ö×Ó | |
| B£® | Ēč·Ö×ÓÖŠĢ¼ĒčČż¼ü¼ü³¤“óÓŚŅŅČ²ÖŠĢ¼Ģ¼Čż¼ü¼ü³¤£¬ĖłŅŌĒčĘųøüČŻŅ×ŗĶĒāĘų¼Ó³É | |
| C£® | ĒčĘųÄÜÓėĒæ¼īČÜŅŗ·“Ó¦µĆµ½Ēč»ÆĪļŗĶ“ĪĒčĖįŃĪ | |
| D£® | Ēč·Ö×ÓÖŠ¦Ņ¼üŗĶ¦Š¼üµÄøöŹż±ČĪŖ3£ŗ4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ō×Ó°ė¾¶£ŗW£¾R£¾Y£¾Z£¾X | |
| B£® | X”¢YŗĶZČżÖÖŌŖĖŲŠĪ³É»ÆŗĻĪļÖŠŅ»¶Øŗ¬ÓŠĄė×Ó¼üŗĶ¹²¼Ū¼ü | |
| C£® | ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗZ£¾Y£¾R | |
| D£® | YµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļŅ»¶ØÓŠĒæµÄŃõ»ÆŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ż | B£® | ¢Ł¢Ū¢Ż | C£® | ¢Ś¢Ü¢Ž | D£® | ¢Ū¢Ż¢Ž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com