
(本题6分)Ⅰ.在某压强恒定的密闭容器中加入2 mol N2和4 mol H2,发生如下反应: N2(g)+3H2(g)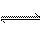 2NH3(g);ΔH=-92.4 kJ·mol-1。达到平衡时,体积为反应前的三分之二。求:
2NH3(g);ΔH=-92.4 kJ·mol-1。达到平衡时,体积为反应前的三分之二。求:
(1)达到平衡时,N2的转化率为____________。
(2)若向该容器中加入a mol N2、b mol H2、c mol NH3,且a、b、c均大于0,在相同条件下达到平衡时,混合物中各组分的物质的量与上述平衡相同。试比较反应放出的能量:(1)__________(2)(填“>”“<”或“=”)。
Ⅱ.若将2 mol N2和4 mol H2放入起始体积相同的恒容容器中,在与Ⅰ相同的温度下达到平衡。试比较平衡时NH3的浓度:Ⅰ____________Ⅱ(填“>”“<”或“=”)。
Ⅰ.(1)50% (2)> Ⅱ.>
【解析】
试题分析:Ⅰ.(1)体积之比等于物质的量之比,故平衡后反应混合气体总的物质的量为(2mol+4mol)× =4mol,则:N2(g)+3H2(g)?2NH3(g) 物质的量减6mol-4mol=2mol故n(N2)=1mol,氮气的转化率=
=4mol,则:N2(g)+3H2(g)?2NH3(g) 物质的量减6mol-4mol=2mol故n(N2)=1mol,氮气的转化率= ×100%=50%,故答案为:50%;(2)开始加入a mol N2、b mol H2、c mol NH3,在相同条件下达到平衡时,混合物中各组分的物质的量与原平衡相同,为等效平衡,按化学计量数转化到左边满足氮气为2mol、氢气为4mol,(2)中由于氨气存在,故参加反应的氮气的物质的量比(1)中少,所以放出的热量(1)>(2),故答案为:>;Ⅱ.若将2molN2和4molH2放入起始体积相同的恒容容器中,在与Ⅰ相同的温度下达到平衡,等效为在Ⅰ平衡基础上增大体积降低压强,平衡时浓度混合气体浓度降低,平衡时NH3的浓度:Ⅰ>Ⅱ,故答案为:>
×100%=50%,故答案为:50%;(2)开始加入a mol N2、b mol H2、c mol NH3,在相同条件下达到平衡时,混合物中各组分的物质的量与原平衡相同,为等效平衡,按化学计量数转化到左边满足氮气为2mol、氢气为4mol,(2)中由于氨气存在,故参加反应的氮气的物质的量比(1)中少,所以放出的热量(1)>(2),故答案为:>;Ⅱ.若将2molN2和4molH2放入起始体积相同的恒容容器中,在与Ⅰ相同的温度下达到平衡,等效为在Ⅰ平衡基础上增大体积降低压强,平衡时浓度混合气体浓度降低,平衡时NH3的浓度:Ⅰ>Ⅱ,故答案为:>
考点:化学平衡的计算


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源:2014秋浙江省杭州地区六校高二上学期期中考试化学试卷(解析版) 题型:选择题
在一定温度下的刚性密闭容器中,当下列哪些物理量不再发生变化时,表明下述反应:
A(s)+2B(g)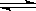 C (g)+D(g) 已达到平衡状态的是
C (g)+D(g) 已达到平衡状态的是
混合气体的压强,②C的物质的量浓度,③A的物质的量,
④2υ正( B) =υ逆(C ),⑤混合气体的平均相对分子质量
A.②④⑤ B.②③④ C.①②③ D.②③⑤
查看答案和解析>>
科目:高中化学 来源:2014秋浙江省杭州地区六校高一上学期期中考试化学试卷(解析版) 题型:选择题
“玉兔”号月球车用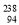 Pu作为热源材料。下列关于
Pu作为热源材料。下列关于 Pu的说法正确的是
Pu的说法正确的是
A. Pu与
Pu与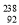 U互为同位素
U互为同位素
B. Pu与
Pu与 Pu为同一种核素
Pu为同一种核素
C. Pu与
Pu与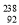 U具有完全相同的化学性质
U具有完全相同的化学性质
D. Pu与
Pu与 Pu具有相同的最外层电子数
Pu具有相同的最外层电子数
查看答案和解析>>
科目:高中化学 来源:2014秋河北省、临漳一中、永年二中高二上学期期中联考化学试卷(解析版) 题型:选择题
、稀氨水中存在着下列平衡:NH3·H2O NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入适量的物质是
NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入适量的物质是
A、NH4Cl B、硫酸 C、NaOH固体 D、水
查看答案和解析>>
科目:高中化学 来源:2014秋河北省、临漳一中、永年二中高二上学期期中联考化学试卷(解析版) 题型:选择题
设C+CO2?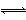 ?2CO ΔH>0的反应速率为v1,N2 +3H2
?2CO ΔH>0的反应速率为v1,N2 +3H2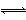 ??2NH3 ΔH<0的反应速率为v2,对于上述反应,当温度升高时,v1和v2的变化情况为
??2NH3 ΔH<0的反应速率为v2,对于上述反应,当温度升高时,v1和v2的变化情况为
A.同时增大 B.同时减小
C.v1增大,v2减小 D.v1减小,v2增大
查看答案和解析>>
科目:高中化学 来源:2014秋河北省高二上学期期中化学试卷(解析版) 题型:选择题
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2(g)+3H2(g)  2NH3(g)ΔH=-92.4kJ·mol
2NH3(g)ΔH=-92.4kJ·mol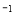 ),下列说法错误的是
),下列说法错误的是
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
NH3的平衡浓度(mol·L | c1 | c2 | c3 |
反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
体系压强(Pa) | p1 | p2 | p3 |
反应物转化率 | a1 | a2 | a3 |
A.2c1<c3 B.a+b=92.4
C.a1+a3<1 D.p3>2p2=2p1
查看答案和解析>>
科目:高中化学 来源:2014秋河北省高二上学期期中化学试卷(解析版) 题型:选择题
在一个固定容积的密闭容器中,加入a molA、b molB,发生aA(g)+bB(g) pC(g),且a+b≠p,则处于平衡状态的标志是
pC(g),且a+b≠p,则处于平衡状态的标志是
A.c(A)=c(B)=c(C)
B.单位时间消耗a molA同时消耗b molB
C.混合气体的压强保持不变
D.混合气体的密度保持不变
查看答案和解析>>
科目:高中化学 来源:2014秋河北省高二上学期期中化学试卷(解析版) 题型:选择题
下面是四位同学在学习“化学反应的速率和化学平衡”一章后,联系工业生产实际所发表的观点,你认为不正确的是
A.使用冰箱保存食物,是利用了化学反应速率理论
B.化学平衡理论是研究怎样使用有限原料多出产品
C.使用催化剂,可加快反应速率,目的是提高生产效率
D.化学反应速率理论是研究怎样提高原料转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com