
【题目】下列“实验结论”与“实验操作及现象”相符的一组是( )
选项 | 实验操作及现象 | 实验结论 |
A | 向紫色石蕊溶液中加入氯水,溶液先变红,随后褪色 | 氯水中含有酸性物质和漂白性物质 |
B | 向某溶液中加入盐酸,产生能使澄清石灰水变浑浊的气体 | 该溶液中一定含有CO |
C | 向某溶液中加入AgNO3溶液,产生白色沉淀 | 该溶液中一定含有Cl- |
D | 向蔗糖中滴加浓硫酸,蔗糖变黑 | 浓硫酸有吸水性 |
A.AB.BC.CD.D
【答案】A
【解析】
A.氯气溶于水生成HClO和HCl,溶液显酸性,因此石蕊溶液会变红,而HClO有强氧化性,所以后面溶液又褪色,A符合题意;
B.除了CO32-,若溶液中存在HCO3-或SO32-或HSO3-,加入盐酸,也能产生使澄清石灰水变浑浊的气体(CO2或SO2),所以该溶液中可能含有CO32-, B不符合题意;
C.向溶液中加入AgNO3溶液,产生白色沉淀,该沉淀可能是:AgCl或Ag2CO3,所以该溶液中可能含有Cl-,若题目改为“向溶液中加入硝酸酸化的AgNO3溶液,产生白色沉淀”,因为硝酸会排除CO32-的干扰,所以该溶液中一定含有Cl-,该沉淀为AgCl,C不符合题意;
D.向蔗糖中滴加浓硫酸,蔗糖变黑,说明浓硫酸具有脱水性,使蔗糖脱水生成炭而变黑,D不符合题意;
答案选A。


科目:高中化学 来源: 题型:
【题目】某氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如图所示步骤进行操作。下列说法中正确的是( )
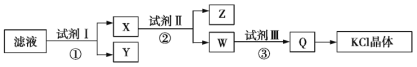
A. 始滤液的pH=7
B. 试剂Ⅰ为Ba(NO3)2溶液
C. 步骤②中加入试剂Ⅱ的目的是除去Ba2+
D. 图示步骤中的2次过滤操作不可以合并
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种可溶性盐,阳离子分别可能是Ba2+、Na+、Ag+、Cu2+中的某一种,阴离子分别可能是![]() 中的某一种。
中的某一种。
(1) C的溶液呈蓝色,向这四种盐溶液中分别加盐酸,B盐有沉淀产生,D盐有无色无味气体逸出。则它们的化学式应为:
A_______,B_______,C_______,D_______。
(2)写出下列反应的离子方程式:
①A+C__________________________。
②D+盐酸________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素a--f在周期表中的位置如表所示,下列有关说法正确的是
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
二 | c | d | |||||
三 | a | b | e | f |
A. c、d、e的氢化物中,e的氢化物沸点最高
B. a、b、d三种元素的离子半径:a >b >d
C. 六种元素中,a元素的金属性最强
D. e、f的氧化物对应的水化物的酸性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语表示正确的是
A. 羟基的电子式:![]()
B. 甘氨酸的结构简式:C2H5NO2
C. AlCl3溶液中Al3+水解的离子方程式:Al3++3H2O![]() Al(OH)3+3H+
Al(OH)3+3H+
D. 粗铜(含Cu及少量Zn、Fe、Ag等)电解精炼时,阳极主要发生反应:Ag-e-=Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. Ag2SO4固体与饱和NaCl溶液反应:Ag2SO4+2Cl-=2AgCl+SO42-
B. 用惰性电极电解饱和NH4Cl溶液:2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
C. NaAlO2溶液中通入过量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
D. KMnO4酸性溶液与FeSO4溶液反应:MnO4-+Fe2++8H+=Mn2++Fe3++4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是功能性高分子材料的单体,化合物Y是一种抗菌药物,它们的结构简式如下图所示:
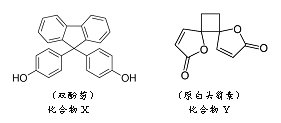
下列说法错误的是
A. X、Y均能与浓Br2水发生反应
B. X分子中四个苯环处于同一平面
C. X、Y分子中手性碳原子数依次为1个、2个
D. 1molX、1molY分别与NaOH反应时,最多消耗NaOH的物质的量均为2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜的化合物用途非常广泛。已知下列反应:[Cu(NH3)2]++NH3+CO![]() [Cu(NH3)3CO]+,2CH3COOH+2CH2=CH2+O2
[Cu(NH3)3CO]+,2CH3COOH+2CH2=CH2+O2![]() 2CH3COOCH=CH2+2H2O。
2CH3COOCH=CH2+2H2O。
(1)Cu2+基态核外电子排布式为____。
(2)NH3分子空间构型为____。
(3)CH3COOCH=CH2分子中碳原子轨道的杂化类型是_____,1molCH3COOCH=CH2中含![]() 键数目为____。
键数目为____。
(4)CH3COOH可与H2O混溶,除因为它们都是极性分子外,还因为_______。
(5)配离子[Cu(NH3)3CO]+中NH3及CO中的C与Cu(Ⅰ)形成配位键。不考虑空间构型,[Cu(NH3)3CO]+的结构可用示意图表示为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
A. 1 L 1 mol/L的Na2CO3溶液中含有的CO32-数目为![]()
B. 常温常压下,8 g O2含有的电子数是4NA
C. 标准状况下,2.24 L CCl4中含有的分子数为0.1NA
D. 25℃时,1 L pH=13的 Ba(OH)2溶液中含有的OH-数目为0.2![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com