
| A. | 丙烷的一氯代物有2种,丙烷的二氯代物有4种 | |
| B. | 分子式为C8H10,且属于芳香族化合物的同分异构体只有3种 | |
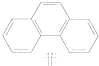
| C. | 菲的结构简式如右图,它与硝酸反应,所得一硝基取代物有5种 | |
| D. | 甲苯苯环上的一个氢原子被一C3H7取代,所得有机产物有6种 |
分析 A.一氯取代物的同分异构体,就是分子中能够被取代的H的种类;利用定一移二法确定二氯代物的同分异构体数目,写出一氯代物,再根据分子中含有H原子种类,判断二氯代物的数目;
B.分子式为C8H10,且属于芳香族化合物,分子中含有1个苯环,侧链为烷基,若有1个侧链,为-CH2-CH3;若有2个侧链,为-CH3,有邻、间、对3种;
C.根据苯环等效H判断;
D.先判断可能的烷基异构情况,利用等效H判断甲苯苯环上的H原子种类有3种,据此判断.
解答 解:A.丙烷分子中有2种H原子,其一氯代物有2种,为CH3CH2CH2Cl,CH3CH(Cl)CH3,CH3CH2CH2Cl中含有3种H原子,再次一氯取代有3种产物,CH3CH(Cl)CH3中含有2种H原子,再次一氯取代有2种产物,其中有两种为同一物质,故丙烷的二氯代物有4种,故A正确;
B.分子式为C8H10,且属于芳香族化合物,分子中含有1个苯环,侧链为烷基,若有1个侧链,为-CH2-CH3;若有2个侧链,为-CH3,有邻、间、对3种,故符合条件的结构共有4种,故B错误;
C. 为对称结构,有如图所示的5种H原子
为对称结构,有如图所示的5种H原子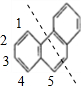 ,所以与硝酸反应,可生成5种一硝基取代物,故C正确;
,所以与硝酸反应,可生成5种一硝基取代物,故C正确;
D.当-C3H7为正丙基,甲苯苯环上的H原子种类有3种,所以有3种同分异构体.当-C3H7为异丙基,甲苯苯环上的H原子种类有3种,所以有3种同分异构体,故所得有机产物共有6种,故D正确;
故选B.
点评 本题考查同分异构体的书写与判断,题目难度中等,注意明确烷基的异构与等效H的判断方法:①同一碳原子上的氢原子是等效的,②同一碳原子上所连接甲基上的氢原子是等效的,③处于同一对称位置的碳原子上的氢原子是等效的.


科目:高中化学 来源:2017届河南省开封市高三上学期10月定位考试化学试卷(解析版) 题型:选择题
为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
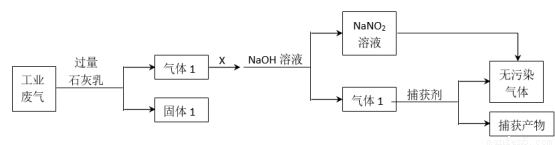
下列说法错误的是
A.固体1中主要含有Ca(OH)2、CaCO3、CaSO3
B.X可以是空气,且需过量
C.捕获剂所捕获的气体主要是CO
D.处理含NH4+废水时,发生反应的离子方程式为:NH4++NO2-=N2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
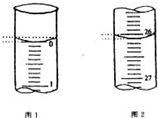 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol/L 盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.10 | 26.10 |
| 第二次 | 25.00 | 1.56 | 28.08 | 26.52 |
| 第三次 | 25.00 | 0.22 | 26.34 | 26.12 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
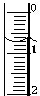 某化学兴趣小组使用酸碱中和滴定法测定市售白醋的总酸量(g/100mL).
某化学兴趣小组使用酸碱中和滴定法测定市售白醋的总酸量(g/100mL).| 滴定次数 实验数据(mL) | 1 | 2 | 3 | 4 |
| V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1NaNO3溶液:H+、Fe2+、Cl-、SO42-、K+ | |
| B. | $\frac{{K}_{W}}{c({H}^{+})}$=10-13mol•L-1的溶液:Na+、AlO2-、OH-、NO3- | |
| C. | 0.1 mol•L-1NH3•H2O溶液:K+、Na+、NO3-、C1- | |
| D. | 加入铝粉能产生大量H2的溶液:Na+、K+、Cl-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
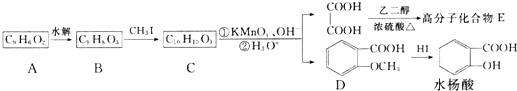
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24 L CHCl3的原子总数为0.1 NA | |
| B. | 1mol-OH所含的电子数为10NA | |
| C. | 常温常压下,28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2 NA | |
| D. | 常温常压下,1mol丙烷所含有的共价键数目为12NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NA个Al(OH)3胶体粒子的质量为78g | |
| B. | 8.0 g Cu2S和CuO的混合物中含有铜原子数为0.1NA | |
| C. | 在0.1mol•L-1的碳酸钠溶液中,阴离子总数一定大于0.1NA | |
| D. | 标准状况下,2.24 L己烷中共价键数目为1.9NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com