
| A、①②③④ | B、④①②③ |
| C、①④②③ | D、①④③② |


科目:高中化学 来源: 题型:
| A、2 6 4 2 3 8 |
| B、2 4 3 2 2 6 |
| C、2 0 1 2 0 2 |
| D、2 2 2 2 1 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 出发来合成A,其合成路线如图:
出发来合成A,其合成路线如图:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、区别苯和乙苯:加酸性高锰酸钾溶液,振荡,观察现象 |
| B、检验无水乙醇中是否含有少量水:加硫酸铜晶体观察现象 |
| C、乙醇的消去反应、皂化反应、淀粉的水解反应均可用浓硫酸作催化剂 |
| D、检验氯代烃中的氯元素时,可先加氢氧化钠溶液加热,再加入硝酸溶液,最后加入硝酸银溶液来进行检验 |
查看答案和解析>>
科目:高中化学 来源: 题型:
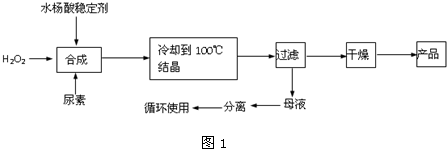
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除去乙醛中的乙酸杂质:加入氢氧化钠溶液洗涤,分液 |
| B、检验乙醇中是否含水:用无水硫酸铜,观察是否变蓝色 |
| C、鉴别SO2和Cl2:通入品红溶液,观察是否褪色 |
| D、获得NH4Cl晶体:将NH4Cl溶液蒸发浓缩,冷却结晶,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
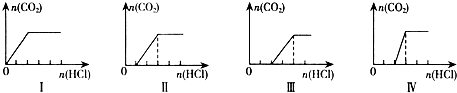
| 溶质的成份 | 对应的图象 | 原溶液中离子浓度关系 | |
| A | NaHCO3 | Ⅰ | c(Na+)=c(HCO3-) |
| B | NaHCO3、Na2CO3 | Ⅱ | c(CO32-)<c(HCO3-) |
| C | NaOH、Na2CO3 | Ⅲ | c(OH-)>c(CO32-) |
| D | Na2CO3 | Ⅳ | c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| A、Ⅰ | B、Ⅱ | C、Ⅲ | D、Ⅳ |
查看答案和解析>>
科目:高中化学 来源: 题型:
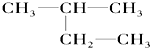 ③金刚石④
③金刚石④35 17 |
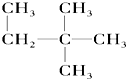 ⑥
⑥ ⑦
⑦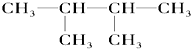 ⑧氯气 ⑨石墨 ⑩
⑧氯气 ⑨石墨 ⑩37 17 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| 投料比[n(H2)/n(CO2)] | 500K | 600K | 700K | 800K |
| 1.5 | 45% | 33% | 20% | 12% |
| 2.0 | 60% | 43% | 28% | 15% |
| 3.0 | 83% | 62% | 37% | 22% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com