
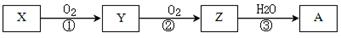
| A.若X为N2或NH3(催化氧化),则A为硝酸 |
| B.若X为S 或H2S(完全燃烧),则A为硫酸 |
| C.若X为非金属单质或非金属氢化物,则A不一定能与金属铜反应生成Y |
| D.反应①和②一定为氧化还原反应,反应③一定为非氧化还原反应 |
 2NO,4NH3+5O2
2NO,4NH3+5O2 4NO+6H2O;2NO+O2=2NO2;3NO2+ H2O = 2HNO3+ NO。则A为硝酸,正确。B.若X为S 或H2S(完全燃烧),S+ O2
4NO+6H2O;2NO+O2=2NO2;3NO2+ H2O = 2HNO3+ NO。则A为硝酸,正确。B.若X为S 或H2S(完全燃烧),S+ O2 SO2;2H2S+ 3O2
SO2;2H2S+ 3O2 2SO2+ 2H2O;2SO2+ O2
2SO2+ 2H2O;2SO2+ O2 2SO3;SO3+H2O= H2SO4则A为硫酸。正确。C.若X为非金属单质或非金属氢化物,如C或CH4,则它们发生不完全燃烧产生CO,CO燃烧得到CO2,CO2容易水产生的是碳酸,则碳酸不能与金属铜反应生成CO。若X是S或H2S,反应得到的浓硫酸与Cu在加热时可以反应得到SO2。因此A不一定能与金属铜反应生成Y。正确。D.反应①和②一定为氧化还原反应,反应③可能为氧化还原反应3NO2+ H2O = 2HNO3+ NO,也可能是非氧化还原反应如SO3+H2O= H2SO4。错误。
2SO3;SO3+H2O= H2SO4则A为硫酸。正确。C.若X为非金属单质或非金属氢化物,如C或CH4,则它们发生不完全燃烧产生CO,CO燃烧得到CO2,CO2容易水产生的是碳酸,则碳酸不能与金属铜反应生成CO。若X是S或H2S,反应得到的浓硫酸与Cu在加热时可以反应得到SO2。因此A不一定能与金属铜反应生成Y。正确。D.反应①和②一定为氧化还原反应,反应③可能为氧化还原反应3NO2+ H2O = 2HNO3+ NO,也可能是非氧化还原反应如SO3+H2O= H2SO4。错误。

 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案科目:高中化学 来源:不详 题型:单选题
| A.久置的氯水能使有色布条褪色 |
| B.向NaHCO3固体加入新制氯水,有无色气体产生 |
| C.向FeCl2溶液中滴加新制氯水,再滴加KSCN溶液,呈血红色 |
| D.在新制氯水中滴加AgNO3溶液有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
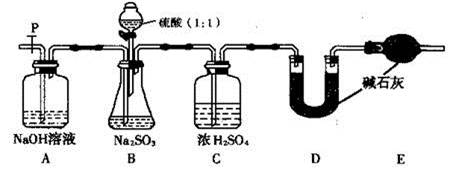
| 实验操作 | 现象和结论 |
| 步骤1:取少许样品于试管中,加入适量蒸馏水充分溶解,再滴加H2SO4酸化的KMnO4溶液; | 现象:若KMnO4溶液的紫红色褪为无色 ①结论:样品中有 离子,假设1不成立。 ②褪色的离子方程式为: 。 |
| 步骤2:另取少许样品于试管中,加入适量蒸馏水充分溶解,再滴加稀HCl,使溶液呈酸性,再滴加适量BaCl2溶液; | ③现象:若 ; 结论:假设2成立。 |
| …… | …… |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.X可能含有2种盐 | B.a是SO3 |
| C.Y可能含(NH4)2SO4 | D.(NH4)2S2O8中S元素的化合价不可能为+7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 | |
| 第一次称量 | 第二次称量 | ||
| 11.710g | 22.700g | 18.621g | a |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
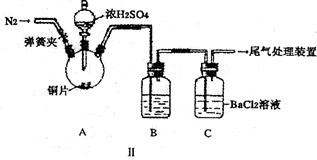
| | 酸 | 实验结果 |
| a | 浓硫酸 | 加热后发生反应,产生无色刺激性气体 |
| b | 稀硫酸 | 加热也不发生反应 |
| c | 浓硝酸 | 不加热即发生反应,产生红棕色气体 |
| d | 稀硝酸 | 微热发生反应,产生无色气体 |


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SO2能使品红溶液褪色是因为SO2具有氧化性,所以它也能使酸碱指示剂褪色 |
| B.硫化氢中硫显最低价态-2价,因此只具有还原性 |
| C.浓硫酸使木棒或棉花变黑,体现了浓硫酸的吸水性 |
| D.BaSO4可作“钡餐”进行X射线检查 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com