
| A、滴加甲基橙试剂显红色的溶液中:Na+、Fe2+、Cl-、NO3- |
| B、水电离出的c(H+)=10-12mol/L的溶液中:K+、Na+、SO4 2-、AlO2- |
| C、能与铝反应生成氢气的溶液中:Mg2+、Na+、Cl-、NO3- |
| D、滴入KSCN显血红色的溶液中:NH4+、Mg2+、SO42-、Cl- |


科目:高中化学 来源: 题型:
| A、V3>V2>V1 |
| B、V3=V2=V1 |
| C、V3>V2=V1 |
| D、V1=V2>V3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸镁与H2SO4反应:MgCO3+2H+=Mg2++H2O+CO2↑ |
| B、向硝酸银溶液中加盐酸:Ag++Cl-=AgCl↓ |
| C、铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| D、澄清石灰水与盐酸的反应:H++OH-=H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 理论阐述 | 评价 |
| A | 醋酸钠溶于水显碱性:CH3COO-+H2O=CH3COOH+OH- | 正确 |
| B | 由于偏铝酸钠溶液中存在:AlO2-+2H2O?Al(OH)3+OH- 因此,将偏铝酸钠溶液加热蒸干得到Al(OH)3沉淀 |
正确 |
| C | 处于弱酸性环境下的钢铁被腐蚀,是因为负极处产生H2,正极处吸收O2 | 正确 |
| D | 将钢闸与外加电源正极相连,是牺牲阳极的阴极保护法, | 错误 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(H+)随着温度的升高而降低 |
| B、35℃时,c(H+)<c(OH-) |
| C、35℃时的水比25℃时的水电离程度小 |
| D、水的电离是吸热的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3CH(C2H5)CH3 2-乙基丙烷 |
| B、CH3CH2CH2CH2OH 1-丁醇 |
C、 间二甲苯 间二甲苯 |
D、 2-甲基-2-丙烯 2-甲基-2-丙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
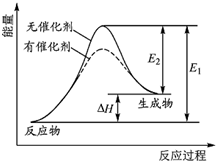 某反应的反应过程中能量变化如图所示(图中E表示活化能),下列叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E表示活化能),下列叙述正确的是( )| A、逆反应的活化能大于正反应的活化能 |
| B、该反应为放热反应 |
| C、催化剂能改变反应的焓变 |
| D、催化剂能降低反应的活化能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
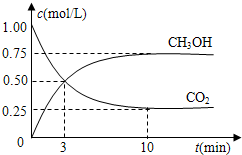 在体积为1L的密闭容器中(体积不变),充入1mol CO2和3mol H2,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)测得CO2和CH3OH(g)的浓度随时间变化如图.
在体积为1L的密闭容器中(体积不变),充入1mol CO2和3mol H2,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)测得CO2和CH3OH(g)的浓度随时间变化如图.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com