
【题目】下列物质性质与用途具有对应关系的是
A.氨气易液化,可用作制冷剂
B.溴化银具有感光性,可用于人工降雨
C.氯化铁具有氧化性,可用了自来水的杀菌消毒
D.氢氧化铝能与氢氧化钠反应,可用于治疗胃酸过多
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A. 碳酸氢钠溶液与过量的澄清石灰水反应:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O
B. 酸性KMnO4溶液与H2O2反应:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O
C. 硫酸溶液与氢氧化钡溶液混合:H++SO42-+Ba2++OH-=BaSO4↓+ H2O
D. 氯气溶于水:Cl2+ H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于酸、碱、盐元素组成的说法中,正确的是( )
A.酸、碱一定含有氢,盐一定不含氢
B.酸、碱、盐可能都不含金属元素
C.碱、盐可能含氧,酸一定含氧
D.盐、碱一定含有金属元素,酸一定不含金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是周期表中短周期的一部分,A、B、C三种元素的原子核外电子数等于B的质量数,B元素的原子核内质子数等于中子数,下列叙述正确的是( )
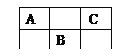
A. B为第二周期的元素
B. C为VA族元素
C. 三种元素都为金属元素
D. C所形成的气态氢化物是三种元素中最稳定的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作会使配制的氢氧化钠溶液的物质的量浓度偏高的是( )
A. 所用氢氧化钠已经潮解
B. 向容量瓶中加水,未到至刻度线
C. 没有洗涤烧杯及玻璃棒2~3次
D. 称量时,氢氧化钠固体和砝码放错托盘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.铈、铬、钛、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用。
(1)二氧化铈(CeO2)在平板电视显示屏中有着重要应用。CeO2在稀硫酸和H2O2的作用下可生成Ce3+,CeO2在该反应中作___________剂。
(2)自然界的Cr主要以+3价和+6价(Cr2O72-)存在。+6价的Cr能引起细胞的突变,可以用亚硫酸钠将其还原为Cr3+。写出该离子方程式:_________________________________。
(3)钛(Ti)被誉为“二十一世纪的金属”,工业上在550℃时用钠与四氯化钛反应可制得钛,该反应的化学方程式是____________________________________。
II.(NH4)2Fe(SO4)2·6H2O(莫尔盐,浅绿色)用作化学试剂、医药以及用于冶金、电镀等。某课题组通过实验检验莫尔盐晶体加热时的分解产物,回答下列问题:
(1)莫尔盐在空气中比硫酸亚铁稳定,但长期露置于空气中也会变质,检验莫尔盐是否变质的试剂是_________________________。
(2)①甲同学提出猜想:分解产物可能是N2、Fe2O3、SO3、H2O四种物质。你是否同意并说明理由:_________________________________________。
②乙同学设计了如图装置,其中装置中的固体变为红棕色,则固体产物中含有___________;
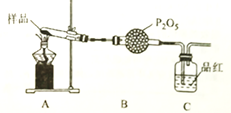
C装置中红色褪去,说明气体产物中含有_______;C装置后应连接尾气吸收装置D,D中盛有的试剂可以是__________________(写一种即可)。
③丙同学想利用上述装罝证明分解产物中含有氨气,只需要更换B和C中的试剂即可,则更换后的试剂为B________________,C_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(硫化碱法是工业上制备Na2S2O3的方法之一,反应原理为:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2(该反应△H>0)。某研究小组在实验室用硫化碱法制备Na2S2O3·5H2O流程如下。
![]()
(1)吸硫装置如图所示
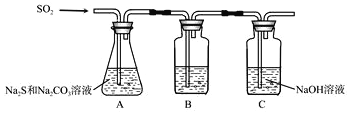
①装置B的作用是检验装置A中SO2的吸收效率,B中试剂是______,表明SO2吸收效率低的实验现象是B中溶液_________。
②为了使SO2尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,除了及时搅拌反应物外,还可采取的合理措施是___________________。(答一条)
(2)假设本实验所用的Na2CO3含少量NaCl、NaOH,设计实验方案进行检验。请完成该实验方案。(已知:室温时CaCO3饱和溶液的pH=10.2)
序号 | 实验操作 | 预期现象 | 结论 |
① | 取少量样品于试管中,加入适量蒸馏水,充分振荡溶解, ______。 | 有白色沉淀生成 | 样品含NaCl |
② | 另取少量样品于烧杯中,加入适量蒸馏水,充分搅拌溶解,_____。 | 有白色沉淀生成,上层清液pH>10.2 | 样品含NaOH |
(3)Na2S2O3溶液是定量实验中的常用试剂,测定其浓度的过程如下:
第一步:准确称取a g KIO3(化学式量:214)固体配成溶液;
第二步:加入过量KI固体和H2SO4溶液,滴加指示剂;
第三步:用Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液的体积为V mL。则c(Na2S2O3)=___mol·L-1。
(4)在(3)的实验中,某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的Na2S2O3浓度可能___________(填“不受影响”、“偏低”或“偏高”),原因是_____________。(用离子方程式表示)。(已知:IO3-+5I-+6H+= 3I2+3H2O,4I-+O2+4H+=I2+2H2O,2S2O32-+I2=S4O62-+2I-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇: CO(g)+2H2(g) ![]() CH3OH(g),现在实验室模拟该反应并进行分析。
CH3OH(g),现在实验室模拟该反应并进行分析。
(1) 下图是该反应在不同温度下CO的转化率随时间变化的曲线。

① 该反应的焓变ΔH__________0(填“>”、“<”或“=”)。
② T1和T2温度下的平衡常数大小关系是K1_______K2(填 “>”、“<”或“=”)。
③ 若容器容积不变,下列措施可增加甲醇产率的是______________。
A. 升高温度 B. 将CH3OH(g)从体系中分离
C. 使用合适的催化剂 D. 充入He,使体系总压强增大
(2)在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考察温度对反应的影响,如图所示

下列说法正确的是________(填序号);
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=![]() mol·L-1·min-1
mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小 ③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时![]() 增大
增大
(3)在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2的转化率为α,则容器内的压强与起始压强之比为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com