
在![]() 、
、![]() 转化为
转化为![]() 的反应中,
的反应中,![]() 的起始浓度为
的起始浓度为![]() ,
,![]() 的起始浓度为
的起始浓度为![]() ,3min后
,3min后![]() 的浓度为
的浓度为![]() 。计算该反应的反应速率是多少?3min 时的
。计算该反应的反应速率是多少?3min 时的![]() 和
和![]() 的浓度各是多少?
的浓度各是多少?
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
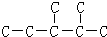 ,此烷烃的一溴代物有
,此烷烃的一溴代物有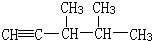
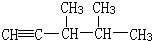
查看答案和解析>>
科目:高中化学 来源: 题型:
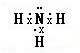
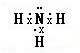
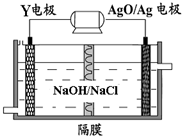
查看答案和解析>>
科目:高中化学 来源: 题型:
 (2013?日照二模)CO、NO、NO2、SO2等都是污染大气的有害气体,对其进行回收利用是节能减排的重要课题.
(2013?日照二模)CO、NO、NO2、SO2等都是污染大气的有害气体,对其进行回收利用是节能减排的重要课题.c(N
| ||
| c(NH3?H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 以下各物质均为中学阶段常见的物质,其中B是单质,它们的转化关系如图所示:
以下各物质均为中学阶段常见的物质,其中B是单质,它们的转化关系如图所示:查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:022
因有机物分子中碳碳双键 不能旋转而产生的同分异构体叫顺反异构体,某些顺反异构体在光的照射下可相互转化,如:
不能旋转而产生的同分异构体叫顺反异构体,某些顺反异构体在光的照射下可相互转化,如:

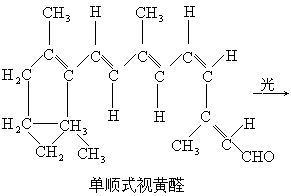

人和高级动物眼睛里的光敏细胞中含有镶嵌在视蛋白中的单顺式视黄醛,在光的作用下转化为全反式视黄醛:
由于全反式视黄醛分子的侧链是“直”的,导致其脱离视蛋白,并由此引起人和动物的视觉受损.
(1)视黄醛分子的顺反异构体共有
[ ]
(2)1mol视黄醛分子与 充分反应时要消耗________
充分反应时要消耗________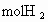 .
.
(3)将视黄醛链端的—CHO还原为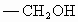 即得维生素A,以下关于维生素A的叙述中正确的是
即得维生素A,以下关于维生素A的叙述中正确的是
[ ]
A.人体缺乏维生素A时易患夜盲症
B.维生素A是易溶于水的醇
C.侧链上的碳原子都在同一平面上
D.所有碳原子都在同一平面上
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com