
| A、浓氨水滴进碱石灰里可制得氨气 |
| B、锌片与稀硝酸反应可制得氢气 |
| C、用乙醇萃取碘水中的碘单质 |
| D、SO2通入溴水,验证SO2的漂白性 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、反应中电子转移数为0.2NA |
| B、一定量的CO2为0.1NA |
| C、18.4 g固体物质为0.1mol Na2CO3和0.1molNa2O2的混合物 |
| D、一定量的Na2O2为0.1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
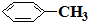 e.
e.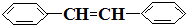 f.
f.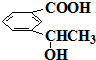
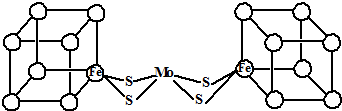
查看答案和解析>>
科目:高中化学 来源: 题型:
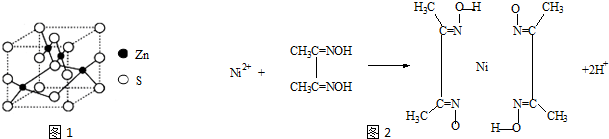
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、干冰可以用于人工降雨 |
| B、推广使用可降解塑料,有助于减少“白色污染” |
| C、将熟石灰和硝酸铵混合施用,肥效更高 |
| D、环境保护应从源头消除污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 溴酸银(AgBrO3)的溶解度随温度变化曲线如图所示,下列说法错误的是( )
溴酸银(AgBrO3)的溶解度随温度变化曲线如图所示,下列说法错误的是( )| A、温度升高时溴酸银溶解速度加快 |
| B、溴酸银的溶解是放热过程 |
| C、60℃时,溴酸银的Ksp约等于6×10-4 |
| D、常温下溴酸银微溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸性强弱:HClO>H2SO4>H2CO3 |
| B、热稳定性:HF>HCl>HBr |
| C、已知硒(Se)与硫同主族,其最高价氧化物对应的水化物分子式为:H2SeO3 |
| D、原子半径大小:Na>P>N |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.9 mol |
| B、1.2 mol |
| C、1.5 mol |
| D、1.8 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、Ba2+、Fe3+、NO3-,通入SO2气体 |
| B、Ca2+、Cl-、K+、H+,通入CO2气体 |
| C、AlO2-、Na+、Br-、SO42-,通入CO2气体 |
| D、HCO3-、Na+、I-、HS-,加入AlCl3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com