
下列有关电解质溶液的说法正确的是
A.向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中 减小
减小
B.在0.1mol·L-1的稀硫酸加水稀释的过程中,c(H+):c(SO42-)始终为2:1
C.向盐酸中加入氨水至中性,溶液中
D.在含0.1mol NaHSO4溶液中:c(H+)=c(SO42-)+c(OH-)
科目:高中化学 来源: 题型:选择题
| A. | 元素丙的单质可用于冶炼金属 | B. | 甲与丁形成的分子中有非极性分子 | ||
| C. | 简单离子半径:丁>乙>丙 | D. | 甲与乙形成的化合物均有氧化性 |
查看答案和解析>>
科目:高中化学 来源:2017届江西省鹰潭市高三上学期第四次月考化学试卷 题型:推断题
芳香酯Ⅰ的合成路线如下:
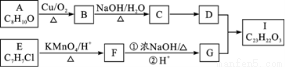
A.C8H16OE.C7H7ClI.C23H22O3
已知以下信息:①A—I均为芳香族化合物,B能发生银镜反应,D的相对分子质量比C大4,E的核磁共振氢谱有3组峰。②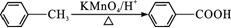
③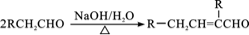
请回答下列问题:
(1)A→B的反应类型为,D所含官能团的名称为,E的名称为。
(2)E→F与F→G的顺序能否颠倒(填“能”或“否”),理由.
(3)B与银氨溶液反应的化学方程式为。
(4)I的结构简式为。
(5)符合下列要求A的同分异构体还有种。
①与Na反应并产生H2②芳香族化合物
(6)根据已有知识并结合相关信息,写出以CH3CH2OH为原料制备CH3CH2CH2CH2OH的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
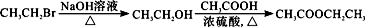
查看答案和解析>>
科目:高中化学 来源:2017届江西省鹰潭市高三上学期第四次月考化学试卷 题型:选择题
用NA表示阿伏伽德罗常数的值,下列叙述正确的是
A.标准状况下,22.4LH2O所含原子个数大于3NA
B.100ml18.4mol/L硫酸与足量Cu反应,生成SO2的分子数为0.92NA
C.t℃时,MgCO3的Ksp=4×10-6,则饱和溶液中含Mg2+数目为2×10-3NA
D.100g质量分数为34.2%的蔗糖分子水溶液中含H原子数为2.2NA
查看答案和解析>>
科目:高中化学 来源:2017届吉林省长春市高三上学期期中考试化学试卷(解析版) 题型:选择题
某恒温密闭容器发生可逆反应Z(?)+W(?) X(g)+Y(?)ΔH,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中正确的是
X(g)+Y(?)ΔH,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中正确的是

A.Z和W在该条件下至少有一个是为气态
B.t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等
C.若该反应只在某温度T0以上自发进行,则该反应的平衡常数K随温度升高而增大
D.若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度不相等
查看答案和解析>>
科目:高中化学 来源:2017届吉林省长春市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.氢气的燃烧热为△H=-285.5kJ•mol-1,则电解水的热化学方程式为2H2O (l) 2H2(g)+O2(g) △H=+285.5k•Jmol-1
2H2(g)+O2(g) △H=+285.5k•Jmol-1
B.反应SO2(g)+2H2S(g)=3S(s)+2H2O(l)在常温下能自发进行,则该反应的△H<0
C.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g)△H=-38.6k•Jmol-1
2NH3(g)△H=-38.6k•Jmol-1
D.由C(石墨,s)=C(金刚石,s)△H=+1.90k•Jmol-1可知,金刚石比石墨稳定
查看答案和解析>>
科目:高中化学 来源:2017届吉林省长春市高三上学期期中考试化学试卷(解析版) 题型:选择题
已知某有机物A分子式为C5H10O2,且能与NaHCO3溶液反应产生气体,则A的同分异构体数目共有(不考虑立体结构)
A.2种
B.3种
C.4种
D.5种
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
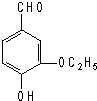
| A. | 1 mol乙基香草醛最多可与1 mol氢气发生加成反应 | |
| B. | 乙基香草醛可与Br2的CCl4溶液发生加成反应 | |
| C. | 1mol乙基香草醛可与含3 mol NaOH的水溶液完全反应 | |
| D. | 乙基香草醛能被酸性高锰酸钾、银氨溶液、新制的氢氧化铜等氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com