
X、Y是短周期同主族元素,Z是过渡元素,化合物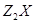 、
、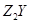 可发生如下转化。
可发生如下转化。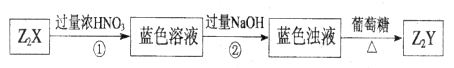
(1)X的元素符号为_________,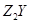 的化学式为_________。
的化学式为_________。
(2)蓝色溶液中含有的阴离子是_______________。
(3)过程②中发生反应的离子方程式为_______________。
(1)S ;Cu2S; (2)NO3—、SO42-、OH-(3)H++OH-=H2O、Cu2++2OH-=Cu(OH)2↓
解析试题分析:X、Y是短周期同主族元素,Z是过渡元素,反应①生成蓝色溶液,则含Cu2+,由蓝色浊液与葡萄糖在加热的条件下反应生成Z2Y,则蓝色浊液为新制氢氧化铜悬浊液, Z2Y为Cu2O,,推出Y为O,X为S,Z为Cu, (1)由上述分析可知,X为S,Z2Y为Cu2O;(2)反应①为硫化亚铜与硝酸的氧化还原反应,反应生成硫酸铜、硝酸铜、NO、水,同时还存在剩余的硝酸,则溶液中的阴离子有NO3-、SO42-、OH-;(3)过程②中发生酸碱中和及铜离子与碱的反应,离子反应分别为H++OH-=H2O、Cu2++2OH-=Cu(OH)2↓。
考点:考查物质推断及相关物质的性质。


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源: 题型:填空题
下列框图中的物质均为中学化学中常见物质,其中甲、乙为单质,其余均为化合物。B为常见液态化合物,A为淡黄色固体,将G的饱和溶液滴入沸水中,煮沸可得到红褐色胶体。请回答下列问题:
(1)A的电子式为 ,乙的组成元素在周期表中的位置是
(2)反应①~⑤中,属于非氧化还原反应的是 (填序号);C中含有的化学键有 (填序号:a离子键; b极性键 ;c 非极性键)
(3)反应⑤的化学方程式为 ;甲与B反应的离子方程式为 。
(4)F溶液中阳离子的检验方法为
(5)在F溶液中加入与F等物质的量的A恰好使F转化为E,写出该反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属。三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有标出)。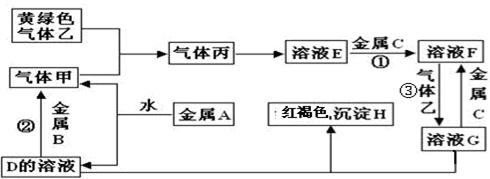
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:F中的溶质 ______________; 丙____________。反应③离子方程式
H受热分解后的固体产物与金属B高温下的化学方程式:_______________________A与水反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。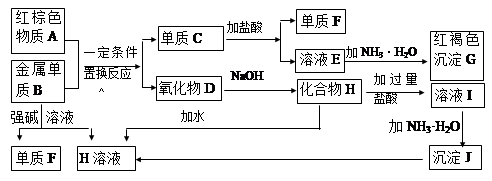
(1)G加热可分解生成A,A的化学式为________,写出物质A的一种用途 。
(2)写出单质B与强碱溶液反应的离子方程式_______________________________________,写出由沉淀J生成 H溶液的离子方程式___________________________________________.。
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式_______________________,白色沉淀L会迅速变为 色,最终变为红褐色沉淀G,写出L变为G的化学反应方程式 。
(4)溶液I中所含金属离子是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
在一定条件下,单质B、C、D、E都能与A单质发生化合反应,转化关系如图所示。已知:①G是黑色晶体,能吸附B单质;②H能与氢氧化钠溶液或盐酸反应;③实验时在G和C的混合物表面加入某强氧化剂粉末,在表面上插入一根除去氧化膜的E片,点燃E引发G与C的反应;④I是绿色植物光合作用的原料,温室中常用它作肥料。根据上述信息,回答下列问题: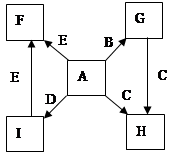

(1)I的电子式为 ,G的俗名是 。
(2)以C和E为电极在NaOH溶液中构成原电池,该原电池的负极反应式为 。
(3)根据E和A反应的能量变化图像写出热化学方程式: 。
(4)两种常见含C元素的盐,一种pH>7,另一种pH<7,写出这两种溶液混合时发生反应的离
子方程式:
(5)写出B在高温下和水蒸气反应的化学方程式并标出电子转移方向和总数 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D、E五种物质均含有同一种元素,它们之间有如下转化关系:
(1)若A为单质,B、C均属于盐类,B的水溶液呈酸性,C的水溶液呈碱性,D是一种白色沉淀。写出下列过程的离子方程式: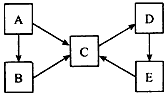
①B的水溶液呈酸性____________。 ②C→D_______________。 ③E→C________________。
(2)若A~E均为化合物。A是淡黄色固体;B、C两溶液在等物质的量浓度时,C 溶液的pH较小。电解D的水溶液是最重要的工业生产之一,D→E→C也是工业制备C的普遍方法。
①A的电子式为__________。
②电解D的水溶液时,反应的离子方程式为________________。
③生铁浸入D溶液而发生锈蚀,正极的电极反应为________________。
(3)若A为单质,C、D的相对分子质量相差16,0.1mol/L E溶液中只有3种离子,且常温下溶液中的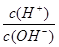 =1012。
=1012。
①B→C的化学方程式为: 。
②A→C的反应中,每转移1 mol e-就会吸热45 kJ,写出该反应的热化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知X、Y、Z为单质,其他为化合物。其中Y为气体,G溶液呈黄色,E是不溶于水的酸性氧化物,能与氢氟酸反应,它们之间存在如下转化关系(部分产物已略去)。请回答下列问题: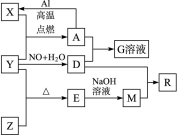
(1)写出物质E的一种用途:__________。
(2)写出A和D的稀溶液反应生成G的离子方程式______________________________。
(3)向含4 mol D的稀溶液中,逐渐加入X粉末至一定量。假设D完全反应且生成的气体只有一种,则反应的X的物质的量范围为___________________ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下图是一些重要工业生产的转化关系(反应条件略去):
请完成下列问题:
(1)若D是单质,且与A属于同一主族,反应在高温下进行,则:
①此反应的化学方程式是 。
②D单质的一种重要用途是 。
(2)若B为黄色固体,D为固体化合物,则该反应为4FeS2+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
①当有1molC生成时,该反应转移电子的总数是 。
②将C通入足量的酸性KMnO4溶液中,发生反应的离子方程式为 。
(3)若B是一种碱性气体,D为化合物,则:
①该反应的化学方程式是 。
②B在加热条件下与CuO反应有Cu生成,该反应的化学方程式为 ;有人提出产物Cu中可能还含有Cu2O。已知Cu+在酸性溶液中不能稳定存在,为验证Cu2O是否存在,可取少量反应产物,滴加足量稀硫酸,若溶液由无色变为蓝色,则证明含有Cu2O。请写出发生反应的化学方程式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下图表示某些化工生产的流程(部分反应条件和产物略去)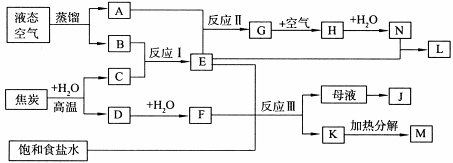
(1)反应Ⅰ需在500℃进行,其主要原因是 。
(2)G转化为H的过程中,需要不断补充空气,其原因是 。
(3)写出反应Ⅲ的化学方程式 。
(4)工业上,向析出K的母液中通氨气,加入细小食盐颗粒,冷却后可析出副产品。通入氨气的作用是 (填序号)。
a.增大NH+4的浓度,使J更多地析出
b.使K更多地析出
c.使K转化为M,提高析出的J的纯度
(5)写出上述流程所涉及的化学工业的名称 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com