
在下图所示的物质转化关系中(反应条件和部分生成物未全部列出),X物质可以来自于海洋中,A、B为常见气体单质,B为黄绿色气体,I、L为常见的金属单质,G为红褐色物质。请回答下列问题:

(1)X化学式为 。 (2)C化学式为 。
(3)反应①的离子方程式为 。
(4)反应②的离子方程式为 。
科目:高中化学 来源: 题型:
甲醇是一种新型的汽车动力燃料,工业上可通过CO(CO的结构式为
C≡O)和H2化合制备甲醇,该反应的热化学方程式为
①CO(g)+2H2(g)====CH3OH(g) ΔH1
该反应的原料CO和H2本身都可作为燃料提供动力,已知这两种物质燃烧的热化学方程式为
②CO(g)+1/2O2(g)====CO2(g) ΔH2=-283 kJ·mol-1
③H2(g)+1/2O2(g)====H2O(g) ΔH3=-242 kJ·mol-1
断开1 mol某些化学键所需的最低能量数据如下表,请回答下 列问题:
列问题:

(1)反应① 的焓变ΔH1=_________。
的焓变ΔH1=_________。
(2)CH3OH(g)燃 烧生成CO2(g)和H2O(g)的热
烧生成CO2(g)和H2O(g)的热 化学方程式为CH3OH(g)+3/2O2(g)
化学方程式为CH3OH(g)+3/2O2(g)
====CO2(g)+2H2O(g) ΔH4,该反应的焓变ΔH4=______________________。
与CO和H2相比,甲醇作为汽车动力燃料的优点是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
以纯锌作阴极,以石墨作阳极,电解某浓度的硫酸锌溶液,阴极产物均附在电极上(阴极产物也不再参加反应损耗),通电一段时间后,关闭电源,迅速撤去电极,若在电解后的溶液中加入4.95 g Zn(OH)2固体,则恰好能使溶液恢复到原浓度,则整个电解过程中,所产生的气体体积为(标准状况) ( )
A.0.56 L B.1.12 L C.2.24 L D.3.36 L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示对应化学反应的离子方程式正确的是
A. 碳酸钙溶于醋酸:CaCO3 + 2H+ = Ca2++ CO2↑+H2O
B.苯酚钠溶液中通入少量的CO2:
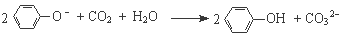
C.用铜做电极电解CuSO4溶液:2Cu2++2H2O 2Cu↓+O2↑+4H+
2Cu↓+O2↑+4H+
D.用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2+ +2OH-
CH3COO-+NH4++3NH3+2Ag↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有H+、NH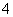 、Mg2+、Fe3+、Al3+、
、Mg2+、Fe3+、Al3+、
SO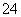 、HCO
、HCO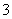 等离子中的一种或几种。当向该溶液中加入一定物质的量的NaOH溶液时,发现生成沉淀的物质的量随加入NaOH溶液的体积变化如下图所示。
等离子中的一种或几种。当向该溶液中加入一定物质的量的NaOH溶液时,发现生成沉淀的物质的量随加入NaOH溶液的体积变化如下图所示。
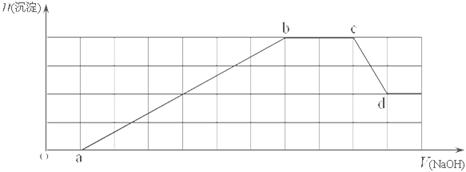
(1)原溶液中一定含有 ,一定不含有 ;
(2)cd段发生的离子反应为 ;
(3)原溶液中物质的量浓度最大的阳离子与原溶液中的阴离子的物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
为了防止枪支生锈,常将枪支的钢铁零件放在NaNO2和NaOH的混合液中进行化学处理使钢铁零件表面生成Fe3O4的致密的保护层——“发蓝”。其过程可用下列化学方程式表示: ① 3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑
② Na2FeO2+ NaNO2+ H2O → Na2Fe2O4+ NH3↑+ NaOH
③ Na2FeO2+Na2Fe2O4+2H2O Fe3O4+4NaOH
Fe3O4+4NaOH
(1)配平化学方程式②。
(2)上述反应①中还原剂为 ,若有1mol Na2FeO2生成,则反应中有 mol电子转移。
(3)关于形成“发蓝”的过程,下列说法正确的是 。
A.该生产过程不会产生污染 B.反应③生成的四氧化三铁具有抗腐蚀作用
C.反应①②③均是氧化还原反应 D.反应①②中的氧化剂均为NaNO2
(4)当NaOH溶液浓度过大,“发蓝”的厚度会变小,其原因是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有等物质的量的铜和银的混合物17.2 g,与50.0 mL
的浓硝酸恰好完全反应,产生气体4.48 L(标准状况),则下列说法正确的是
A.产生的气体是0.2 mol NO2
B.硝酸的物质的量浓度为12 mol·L-1
C.反应中被还原和未被还原的硝酸物质的量之比为3∶2
D.要使产生的气体恰好完全被水吸收需要通入氧气0.075 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
往含0.2 mol NaOH和0.1 mol Ba(OH)2的溶液中持续稳慢地通入CO2气体,使CO2气体充分参加反应,当通入气体为6.72 L(S.T.P)时立即停止,则这一过程中,溶液中离子的物质的量和通入CO2气体的体积关系正确的图像是(气体的溶解忽略不计) ( )
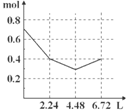

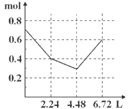
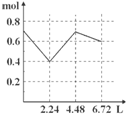
A. B. C. D.
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,向某密闭容器中投入一定量的氮气和氢气,发生反应N2(g)+3H2(g)2NH3(g),下列关于从反应开始至达到化学平衡的过程中正、逆反应速率变化情况的图象中,正确的是( )
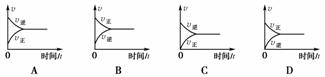
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com