
80℃时,NO2(g)+SO2(g) SO3(g)+NO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入NO2和SO2,起始浓度如下表所示,其中甲经2min达平衡时,NO2的转化率为50%,下列判断不正确的是( )
SO3(g)+NO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入NO2和SO2,起始浓度如下表所示,其中甲经2min达平衡时,NO2的转化率为50%,下列判断不正确的是( )
起始浓度 | 甲 | 乙 | 丙 |
c(NO2)/mol ·L-1 | 0.10 | 0.20 | 0.20 |
c(SO2)/mol ·L-1 | 0.10 | 0.10 | 0.20 |
A. 平衡时,乙中SO2的转化率大于50%
B. 当反应平衡时,丙中c(SO2)是甲中的2倍
C. 温度升至90℃,上述反应平衡常数为25/16,则正反应为吸热反应
D. 其他条件不变,若起始时向容器乙中充入0.10mol ·L-1 NO2和0.20 mol ·L-1 SO2,达到平衡时c(NO)与原平衡不同
科目:高中化学 来源:2016-2017学年福建省高一下学期开学考试化学试卷(解析版) 题型:选择题
下列说法正确的是(NA表示阿伏伽德罗常数)
A. 物质的量浓度为0.5 mol•L-1的MgCl2溶液中,含有Cl-个数为NA
B. 标准状况下,lmol H2所占体积约为22.4L,lmol H2和N2混合气体的体积也约为22.4L
C. 0.1L0.5mol•L-1 CH3COOH溶液中含有的H+数为0.05NA
D. 2.3gNa在足量O2中燃烧,转移的电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源:2017届广西省高三2月月考理综化学试卷(解析版) 题型:填空题
【化学——选修3:物质结构与性质】
(一)硒元素(selenium)是第四周期、第VIA族元素,单质有红硒、黑硒和灰硒,其中灰硒有良好的导热导电性,且有显著的光电效应,可应用于光电半导体材料。请回答下列问题:
(1)Se原子的核外电子排布式为[Ar]_____。
(2)As和Se是同一周期的元素,As的第一电离能比Se大,原因是______。SeO42-中Se―O的键角比SeO3的键角________(填“大”或“小”)。
(3)H2Se比H2S水溶液的酸性强,原因是_____,____。
(4)灰硒的晶体为六方晶胞结构,原子排列为无限螺旋链,分布在六方晶格上,同一条链内原子作用很强,相邻链之间原子作用较弱,其螺旋链状图、晶胞结构图和晶胞俯视图如下。
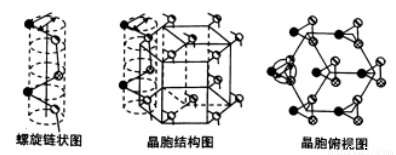
螺旋链中Se原子的杂化方式为____________。
(二)利用CuSO4和NaOH制备的Cu(OH)2检验醛基时,生成红色Cu2O,其晶胞结构如图所示。
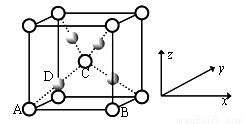
①该晶胞原子坐标参数A为(0,0,0);B为(1,0,0);C为(1/2,1/2,1/2)。则D原子的坐标参数为_________,它代表铜原子。
②若Cu2O晶体密度为d g·cm-3,晶胞参数为a pm,则阿伏加德罗常数值NA=________。
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三2月月考理科综合化学试卷(解析版) 题型:选择题
镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,越来越成为人们研制绿色原电池的关注焦点.其中一种镁原电池的反应为:xMg+Mo3S4 MgxMo3S4,下列说法正确的是( )
MgxMo3S4,下列说法正确的是( )
A. 电池放电时,Mg2+向负极迁移
B. 电池放电时,正极反应为Mo3S4+2xe﹣+xMg2+═MgxMo3S4
C. 电池充电时,阴极发生还原反应生成Mo3S4
D. 电池充电时,阳极反应为xMg﹣2xe﹣═xMg2+
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三下学期期初考试化学试卷(解析版) 题型:填空题
CO2的回收利用对减少温室气体排放、改善人类生存环境具有重要意义。利用CO2和CH4重整可制合成气(主要成分CO、H2),重整过程中部分反应的热化学方程式为: ①CH4(g) = C(s) + 2H2(g) △H = +75.0 kJ·mol-1
②CO2(g) + H2(g) = CO(g) + H2O(g) △H = +41.0 kJ·mol-1
③CO(g) + H2(g) = C(s) + H2O(g) △H = -131.0 kJ·mol-1
(1)反应CO2(g) + CH4(g) = 2CO(g) + 2H2(g)的△H= ___________。
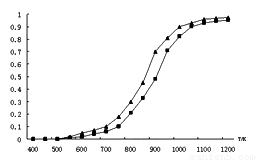
(2)固定n(CO2)= n(CH4),改变反应温度,CO2和CH4的平衡转化率见下图。
①同温度下CO2的平衡转化率 ____________(填“大于”或“小于”)于CH4的平衡转化率,其原因是 __________________________。
②高温下进行该反应时常会因反应①生成“积碳”(碳单质),造成催化剂中毒,高温下反应①能自发进行的原因是_________________。
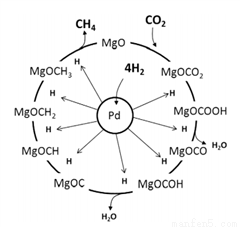
(3)一定条件下Pd-Mg/SiO2催化剂可使CO2“甲烷化”从而变废为宝,其反应机理如图所示,该反应的化学方程式为_____________________,反应过程中碳元素的化合价为-2价的中间体是__________。
(4)卤水可在吸收烟道气中CO2的同时被净化,实现以废治废,其中涉及的一个反应是CaSO4 + Na2CO3 == CaCO3 + Na2SO4,则达到平衡后,溶液中c(CO32-)/c(SO42-) = __________。【用Ksp(CaSO4)和Ksp(CaCO3)表示】
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三下学期期初考试化学试卷(解析版) 题型:选择题
下列图示与对应的叙述相符的是( )
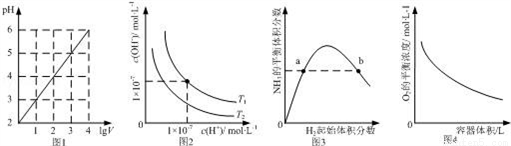
A. 图1表示1 LpH=2的CH3COOH溶液加水稀释至V L,pH随lgV的变化
B. 图2表示不同温度下水溶液中H+和OH﹣浓度的变化的曲线,图中温度T2>T1
C. 图3表示一定条件下的合成氨反应中,NH3的平衡体积分数随H2起始体积分数(N2的起始量恒定)的变化,图中a点N2的转化率小于b点
D. 图4表示同一温度下,在不同容积的容器中进行反应2BaO2(s) 2BaO(s)+O2(g),O2的平衡浓度与容器容积的关系
2BaO(s)+O2(g),O2的平衡浓度与容器容积的关系
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三下学期期初考试化学试卷(解析版) 题型:选择题
下列有关物质的性质与应用相对应的是( )
A. 碳酸钠溶液呈碱性,可用于洗去铁屑表面的油污
B. 铝易发生钝化,可用于作飞机、火箭的结构材料
C. 炭具有还原性,可用于冶炼钠、镁、铝等金属
D. 浓硫酸具有强氧化性,可用于干燥二氧化硫气体
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省长沙市高二下学期第一次模块检测化学试卷(解析版) 题型:选择题
在2A+B 3C+4D反应中,表示该反应速率最快的是
3C+4D反应中,表示该反应速率最快的是
A. υ(A)= 0.5 mol/(L·s) B. υ(B)= 0.3 mol/(L·s)
C. υ(C)= 12 mol/(L·min) D. υ(D)= 6 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三下学期开学考试理综化学试卷(解析版) 题型:选择题
利用如图所示装置(电极均为惰性电极)可吸收SO2,并用阴极排出的溶液吸收NO2,下列说法正确的是
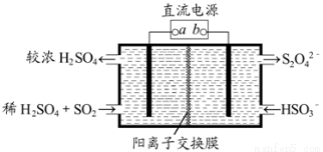
A. a为直流电源的负极
B. 阴极的电极反应式为:2HSO3-+2H2O+2e-=S2O42-+2OH-
C. 阳极的电极反应式为:SO2+2H2O-2e-=SO42-+4H+
D. 电解时,H+由阴极室通过阳离子交换膜到阳极室
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com