
| A. | 可与NaOH溶液反应,1mol该物质可与4mol NaOH反应 | |
| B. | 可与溴水反应,且1mol该物质与足量溴水反应消耗6mol Br2 | |
| C. | 一定条件下1mol该物质可与H2加成,耗H2最大量为7mol | |
| D. | 维生素P遇FeCl3溶液发生显色反应 |
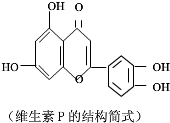
分析 天然维生素P中含有2个苯环,可与氢气发生加成反应,含有的官能团有酚羟基,可发生取代反应,分子中含有C=O,可与氢气发生加成反应,含有C=C,可发生加成、氧化反应,以此解答该题.
解答 解:A.分子中只有4个酚羟基与NaOH反应,其它官能团不参加反应,则1mol该物质可与4molNaOH反应,故A正确;
B.分子中含有2个苯环4个酚羟基,邻位和对位共有5个H原子可被取代,含有1个C=C,可发生加成,则可与溴水反应,且1mol物质与足量溴水反应消耗6molBr2,故B正确;
C.分子中能发生加成反应的有苯环、C=O和C=C,则1mol该物质可与H2加成,耗H2最大量为8mol,故C错误;
D.含有酚羟基,可遇FeCl3溶液发生显色反应,故D正确.
故选C.
点评 本题考查有机物的结构和性质,题目难度不大,本题注意把握官能团的数目的性质,为解答该题的关键.


科目:高中化学 来源: 题型:选择题
| A. | 当锌完全溶解后,铁与酸反应产生氢气的速率会显著减慢,此现象可作为判断镀锌铁皮中锌镀层是否完全被反应掉的依据 | |
| B. | “硝基苯制备”实验中,将温度计插入水浴,水银球不能与烧杯底部和烧杯壁接触 | |
| C. | 在酸碱中和滴定时,右手旋转滴定管的活塞,左手摇动锥形瓶,眼睛看滴定管的液面 | |
| D. | 除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2S+SO2═3S↓+2H2O | B. | Cl2+SO2+2H2O═H2SO4+2HCl | ||
| C. | SO2+2Mg═2MgO+S | D. | SO2+2NaOH═Na2SO3+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 品红的分子式为C20H19N3 | |
| B. | 上述漂白原理反应属加成反应 | |
| C. | 碱性品红及其与H2SO3生成的无色化合物都可与NaOH溶液反应 | |
| D. | 碱性品红与H2SO3生成的无色化合物不稳定,加热后恢复原来的颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镍氢电池、锂离子电池和碱性锌锰干电池都是二次电池 | |
| B. | 燃料电池是一种高效、对环境污染小的新型电池 | |
| C. | 化学电池的反应基础是氧化还原反应 | |
| D. | 铅蓄电池放电的时候负极是Pb正极是PbO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 反应完成后,O2有剩余 | |
| B. | 原混合气体中,C2H4与C2H2的体积共为1.9L | |
| C. | 反应完成后,生成水的质量为9g | |
| D. | 原混合气体中,CO与CH4的体积比一定为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1NaCl溶液中含有0.1nA个Na+ | |
| B. | 标准状况下,22.4 L 苯含有nA个苯分子 | |
| C. | 7.8 g Na2O2与足量水反应转移0.2nA个电子 | |
| D. | 标准状况下,2.24 LCH4和C2H4混合气体中含有的H原子数为0.4nA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com