
分析 设该气体摩尔质量为M,则依据$\frac{m}{M}$=n,计算其摩尔质量,
法一:依据ρ标=$\frac{M}{Vm}$计算;
法二:依据ρ标=$\frac{M}{Vm}$计算氧气的密度,依据阿伏伽德罗定律推论:相同条件下,密度之比等于摩尔质量之比;
法三:计算7g该气体的体积,依据密度公式ρ=$\frac{m}{V}$计算其密度.
解答 解:设该气体摩尔质量为M,则依据$\frac{m}{M}$=n,克某气体和8克氧气所含分子数相同,得:$\frac{7}{M}$=$\frac{8}{32}$,解得M=28(g/mol);
法一:该气体密度:ρ标=$\frac{M}{Vm}$=$\frac{28g/mol}{22.4L/mol}$=1.25g/L;
法二:依据ρ标=$\frac{M}{Vm}$,则氧气的密度ρ(O2)=$\frac{32g/mol}{22.4L/mol}$=1.43g/L,依据阿伏伽德罗定律推论:相同条件下,密度之比等于摩尔质量之比得:$\frac{ρ}{ρ({O}_{2})}$=$\frac{28}{32}$,解得ρ=1.25g/L;
法三:7克某气体和8克氧气所含分子数相同,即二者物质的量相等=$\frac{8g}{32g/mol}$=0.25mol,标况下体积为0.25mol×22.4L/mol=5.6L,则其密度ρ=$\frac{7g}{5.6L}$=1.25g/L;
答:气体的密度为1.25g/L.
点评 本题考查了物质的量的有关计算,涉及气体密度的计算,熟悉以物质的量为核心的计算公式,明确阿伏伽德罗定律推论是解题关键,题目难度中等.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向苏打和小苏打溶液中分别加入盐酸 | 均冒气泡 | 两者均能与盐酸反应 |
| B | 向AgNO3溶液中滴加过量氨水 | 溶液澄清 | Ag+与NH3H2O能大量共存 |
| C | 将可调高度的铜丝伸入到稀NHO3中 | 溶液变蓝 | Cu与稀HNO3发生置换反应 |
| D | 将KI和FeCl3溶液在试管中混合后,加入CCl4,震荡,静置 | 下层溶液显紫红色 | 氧化性:Fe3+<I2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 润洗酸式滴定管时应从滴定管上口加入3~5mL所要盛装的酸溶液,倾斜着转动滴定管,使液体润湿其内壁,再从上口倒出,重复2-3次 | |
| B. | 向酒精灯内添加酒精时,不能多于容积的$\frac{2}{3}$,若不慎洒出的酒精在桌上燃烧,应迅速用水灭火 | |
| C. | 探究温度对反应速率的影响时,应先将硫代硫酸钠溶液、硫酸溶液分别在水浴中加热,然后混合 | |
| D. | 配制浓硫酸和浓硝酸的混合酸时,将浓硝酸沿器壁慢慢加入浓硫酸中,并不断搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
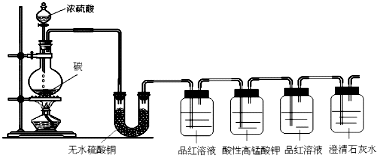
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
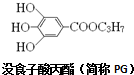
| A. | 没食子酸的分子式为C10H13O5 | B. | 1molPG可与4molNaOH反应 | ||
| C. | PG中的基团-C3H7有两种结构 | D. | PG有还原性,易被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 化学式 | 电离常数 |
| HF | Ki=3.5×10-4 |
| H2CO3 | Ki1=4.3×10-7 |
| Ki2=5.6×10-11 | |
| HClO | Ki=3.2×10-8 |
| A. | 同温同浓度下,溶液的pH值:NaF>NaClO>Na2CO3 | |
| B. | 结合H+的能力:ClO->HCO3->F- | |
| C. | 次氯酸钠溶液中通少量二氧化碳的离子方程式:ClO-+CO2+H2O→HCO3-+HClO | |
| D. | 碳酸钠溶液中加入少量氢氟酸的离子方程式:CO32-+2HF→2F-+H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | C | D |
| ①由C、H、O三种元素组成 ②球棍模型为:  ③能与NH3在一定条件下反应生成丙烯酰胺(CH2=CH-CONH2) | ①由C、H、O三种元素组成 ②能与Na反应,但不能与NaOH溶液反应 ③能与A反应生成相对分子质量为100的酯 | ①相对分子质量与B相同 ②能被弱氧化剂氢氧化铜氧化 ③能与NaHCO3溶液反应放出CO2气体 | ①能使溴的四氯化碳溶液褪色 ②能与水在一定条件下反应生成B |
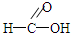 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com