
测血钙的含量时,可将2.0 mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀。将沉淀用稀硫酸处理得H2C2O4后,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+,若终点时用去20.0 mL 1.0×10-4 mol·L-1的KMnO4溶液。
(1)写出用KMnO4滴定H2C2O4的离子方程式 。
(2)判断滴定终点的方法是 。
(3)计算:血液中含钙离子的浓度为 g·mL-1。
(1)2Mn+5H2C2O4+6H+ 2Mn2++10CO2↑+8H2O
2Mn2++10CO2↑+8H2O
(2)当滴入1滴酸性KMnO4溶液后溶液由无色变为浅紫色,且半分钟内不褪色
(3)1.0×10-4
【解析】因为滴加酸性KMnO4溶液至反应完毕过量时,会使溶液呈紫色,故可用滴入一滴酸性KMnO4溶液由无色变为浅紫色且半分钟不褪色的方法来判断终点。由题意知可能发生反应的离子方程式为:2Mn+5H2C2O4+6H+ 2Mn2++10CO2↑+8H2O、Ca2++C2
2Mn2++10CO2↑+8H2O、Ca2++C2 CaC2O4↓、CaC2O4+2H+
CaC2O4↓、CaC2O4+2H+ Ca2++H2C2O4。
Ca2++H2C2O4。
设2 mL血液中含Ca2+的物质的量为x,则
5Ca2+~5CaC2O4~5H2C2O4~2Mn
5 2
x 20.0×10-3 L×1.0×10-4 mol·L-1
x=5.0×10-6 mol,1 mL血液中Ca2+的浓度为=1.0×10-4 g·mL-1。


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源:2014年高二化学人教版选修四 21电解原理练习卷(解析版) 题型:选择题
若某电能与化学能的转化装置(电解池或原电池)中发生的总反应的离子方程式是Cu+2H+ Cu2++H2↑,则下列关于该装置的有关说法中正确的是( )
Cu2++H2↑,则下列关于该装置的有关说法中正确的是( )
A.该装置可能是原电池,也可能是电解池
B.该装置只能是原电池,且电解质溶液为硝酸
C.该装置只能是电解池,且金属铜为该电解池的阳极
D.该装置只能是原电池,电解质溶液不可能是盐酸
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 17难溶电解质的溶解平衡练习卷(解析版) 题型:填空题
(1)在25 ℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成 沉淀(填化学式),生成该沉淀的离子方程式为 。已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,= 。
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 16盐类水解的应用练习卷(解析版) 题型:选择题
在蒸发皿中加热蒸干并灼烧(低于400 ℃)下列物质的溶液,可以得到该固体物质的是( )
A.氯化铝B.碳酸氢钠C.硫酸镁D.高锰酸钾
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 15盐类水解的原理练习卷(解析版) 题型:选择题
相同物质的量浓度的NaCN和NaClO相比,NaCN溶液的pH较大,则下列关于同温、同体积、同浓度的HCN和HClO溶液的说法中正确的是( )
A.酸的强弱:HCN>HClO
B.pH:HClO>HCN
C.与NaOH恰好完全反应时,消耗NaOH的物质的量:HClO>HCN
D.酸根离子浓度:c(CN-)<c(ClO-)
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 14酸碱中和滴定练习卷(解析版) 题型:选择题
用0.1 mol·L-1 NaOH溶液滴定0.1 mol·L-1盐酸,如达到滴定终点时不慎多加了1滴NaOH溶液(1滴溶液的体积约为0.05 mL),继续加水至50 mL,所得溶液的pH是( )
A.4B.7.2C.10D.11.3
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 13pH的计算练习卷(解析版) 题型:选择题
相同体积、相同pH的某一元强酸溶液①和某一元中强酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是( )
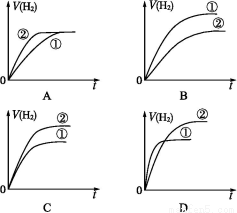
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 11弱电解质的电离练习卷(解析版) 题型:填空题
下表是几种常见弱酸的电离平衡常数(25 ℃)。
酸 | 电离方程式 | 电离平衡常数K |
CH3COOH | CH3COOH | 1.76×10-5 |
H2CO3 | H2CO3 HCO3— | K1=4.4×10-7 K2=4.7×10-11 |
H2S | H2S HS- | K1=1.3×10-7 K2=7.1×10-15 |
H3PO4 | H3PO4 H2PO4— HPO42— | K1=7.1×10-3 K2=6.3×10-8 K3=4.2×10-13 |
回答下列问题:
(1)当温度升高时,K值 (填“增大”“减小”或“不变”)。
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱有何关系?
。
(3)若把CH3COOH、H2CO3、HCO3—、H2S、HS-、H3PO4、H2PO4—、HPO42—都看成是酸,其中酸性最强的是 ,最弱的是 。
(4)多元弱酸是分步电离的,每一步都有相应的电离平衡常数,对于同一种多元弱酸的K1、K2、K3之间存在着一定的规律,此规律是 ,产生此规律的原因是 。
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修二 4单元综合检测练习卷(解析版) 题型:选择题
一包硫酸铵样品中,不慎混入了下列化肥:①氯化铵;②碳酸氢铵;③硝酸钾;④尿素[CO(NH2)2]中的一种。经测定,这种硫酸铵样品中含N的质量分数为23%,则混入的杂质可能是 ( )。
A.①或② B.①或④
C.①或②或③ D.②或③或④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com