
| A. | 将集有氨气的试管倒扣于水槽中,液体迅速充满试管,说明氨气极易溶于水 | |
| B. | 将湿润的红色石蕊试纸放入集有氨气的集气瓶中,试纸由红色变为蓝色,说明氨水呈碱性 | |
| C. | 加热NH4HCO3固体,观察到固体逐渐减少,试管口有液滴产生,说明NH4HCO3受热不稳定 | |
| D. | 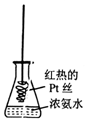 将红热的Pt丝伸入如图所示的锥形瓶中,瓶口出现少量红棕色气体,说明氨气的直接氧化产物为NO2 |
分析 A.氨气极易溶于水,使试管内压强迅速降低;
B.氨气易溶于水,得到的氨水显示碱性;
C.加热NH4HCO3固体,观察到固体逐渐减少,试管口有液滴产生,说明碳酸氢氨受热分解;
D.氨气催化氧化生成一氧化氮,一氧化氮与空气反应生成二氧化氮.
解答 解:A.氨气极易溶于水,使试管内压强迅速降低,液体迅速充满试管,故A正确;
B.将湿润的红色石蕊试纸放入集有氨气的集气瓶中,试纸由红色变为蓝色,说明氨水呈碱性,说明氨水为弱碱,故B正确;
C.加热NH4HCO3固体,观察到固体逐渐减少,试管口有液滴产生,说明碳酸氢氨受热分解,不稳定,故C正确;
D.氨气催化氧化生成一氧化氮,一氧化氮与空气反应生成二氧化氮,故D错误;
故选:D.
点评 本题考查了氨气的性质,熟悉氨气的物理性质、化学性质是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ④⑤⑥ | B. | ①②③④ | C. | ①②④⑥ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 河流三角洲的形成与胶体的性质无关 | |
| B. | 清晨在密林中看到的一缕缕光束,是丁达尔现象的表现 | |
| C. | 向沸水中逐滴加入FeCl3溶液并加热至液体呈透明的红褐色,可得氢氧化铁胶体 | |
| D. | 胶体粒子的直径大小在1~100nm之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入稀盐酸产生无色气体,将气体通入澄淸石灰水,溶液变浑浊,一定有CO32- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入KSCN溶液无明显现象,再加入新制氯水溶液变为血红色,一定有Fe2+ | |
| D. | 加入过量硝酸银溶液,产生白色沉淀,再加入稀盐酸沉淀不溶解,则一定含有C1- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2与CO2反应生成Na2CO3和O2,则Na2O2与SO2反应可生成Na2SO3和O2 | |
| B. | Fe与Cl2反应生成FeCl3,则Fe与I2反应可生成FeI3 | |
| C. | 钠与氧气在不同条件下反应会生成两种不同的氧化物,则Li与氧气反应也能生成Li2O或Li2O2 | |
| D. | Al与Fe2O3能发生铝热反应,则Al与MnO2也能发生铝热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化产物与还原产物分子个数之比为15:1 | |
| B. | 氧化剂和还原剂是同一物质 | |
| C. | 反应过程中转移1mol电子,则产生2.24L气体(标准状况) | |
| D. | NaN3中氮元素的化合价为-3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色)?N2O4g)(无色),如图所示.
在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色)?N2O4g)(无色),如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com