
氨气是一种化工原料。
(1)请写出工业上合成氨的化学方程式:
(2)实验室中,甲、乙两小组选择了不同方法制取氨气,请将实验装置的字母编号和制备原理填写在下表空格中。
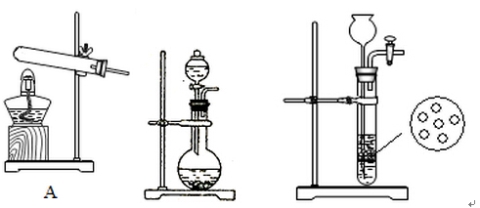
B C
| 实验装置 | 实验药品 | 制备原理 |
甲小组 | A
|
| 反应的化学方程式为 ① |
乙小组 |
| 浓氨水、氢氧化钠固体 | 氢氧化钠的作用:氨水中存在平衡: |
(3)请设计一个操作简单的实验,验证NH3·H2O是弱电解质。
。
(4)甲同学把制得的氨气溶于适量水中,得到稀氨水,用标准浓度的盐酸滴定,测定其浓度。实验步骤:准确量取10.00mL稀氨水于锥形瓶中,加入20mL水稀释,滴加 溶液作为指示剂(填“石蕊”、“酚酞”或“甲基橙”),将 (填“0.020”、“0.05”、“0.1980”或“1.5”)mol?L-1盐酸装入50ml酸式滴定管,滴定至 ,停止滴定,记录数据。重复滴定2次。平均消耗盐酸Vml。计算原稀氨水的物质的量浓度
= (只列出算式,不做运算)
(1) (2分)
(2分)
(2)氢氧化钙固体、氯化铵固体(2分): 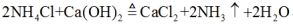 (2分)
(2分)
乙小组:B (1分)
(3)配制NH4Cl溶液,用pH计测量其pH值,若pH值小于7,则NH3·H2O是弱电解质。(2分)
(4)甲基橙 (2分) 0. 1980 (2分) 溶液由黄色变为橙色,且半分钟不恢复原来颜色 (2分)
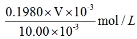 (2分)
(2分)
【解析】
试题分析:(1)工业中用氮气、氢气在高温、高压、催化剂条件下反应生成氨气,化学方程式为
(2)甲选择A装置,说明是用氢氧化钙固体、氯化铵固体加热制取氨气,化学方程式为
2NH4Cl+Ca(OH)2 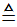 CaCl2+2NH3↑+2H2O;乙组选择浓氨水、氢氧化钠固体制取氨气,不需加热,选择B装置;
CaCl2+2NH3↑+2H2O;乙组选择浓氨水、氢氧化钠固体制取氨气,不需加热,选择B装置;
(3)验证NH3·H2O是弱电解质,只需测定一定浓度的氯化铵溶液的pH,若pH值小于7,说明NH4+水解,则NH3·H2O是弱电解质;
(4)用盐酸滴定氨水,最终溶液呈弱酸性,所以选择甲基橙作指示剂,滴定实验中的数据保持4位有效数字,所以选择盐酸的浓度是0.1980mol/L,甲基橙的变色范围是3.1-4.4,氨水溶液中滴加甲基橙,溶液为黄色,所以当达到滴定终点时,溶液由黄色变为橙色,且半分钟内不恢复。根据氨水与盐酸反应的实质,计算氨水的浓度是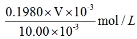 。
。
考点:考查滴定实验操作、计算,制取氨气的不同方法的判断


科目:高中化学 来源:2015届广西桂林市高三上学期第一次月考化学试卷(解析版) 题型:选择题
某反应体系中存在下列六种物质:As2S3、HNO3、H2SO4、NO、H3AsO4和H2O,已知其中As2S3是反应物之一。下列说法不正确的是
A、该反应属于氧化还原反应
B、此反应中只有砷元素被氧化,只有氮元素被还原
C、HNO3、H2O是反应物,H2SO4、NO、H3AsO4是生成物
D、HNO3、H2SO4、H3AsO4都是最高价氧化物对应的水化物
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高三8月月考化学试卷(解析版) 题型:选择题
向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是
| 操作 | 现象 | 结论 |
A | 滴加BaCl2溶液 | 生成白色沉淀 | 原溶液中有SO42- |
B | 滴加氯水和CCl4,振荡、静置 | 下层溶液显紫红色 | 原溶液中有I- |
C | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+、无K+ |
D | 滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
查看答案和解析>>
科目:高中化学 来源:2015届广东省惠州市高三第一次调研考试化学试卷(解析版) 题型:填空题
(16分)钢铁企业酸洗钢材时产生的废液主要成分为Fe2+、H+、Cl-,可用下述方法处理该废液,回收盐酸和制备氧化铁涂料。
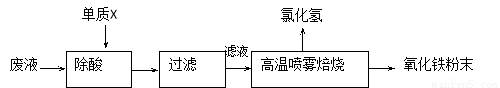
(1)单质X的化学式是 。
(2)氯化亚铁溶液经高温喷雾焙烧转化为HCl气体和氧化铁粉末,有关的化学方程式依次为: 。
(3)某铁红涂料中除含有Fe2O3外,还可能添加有CuO或FeO中的一种,请设计实验方案,探究该铁红涂料中添加物的成分。
① 提出合理假设
假设1:添加了CuO
假设2:添加了FeO
② 请设计方案,验证上述假设,写出实验步骤、预期现象和结论。
限选试剂:铁粉、3mol?L-1H2SO4、0.1 mol?L-1酸性KMnO4溶液、10%NaOH溶液、10%H2O2、KSCN溶液
操作步骤 | 预期现象和结论 |
步骤1.取少量样品于试管中, ____________________________________________
|
样品全部溶解,得到澄清的溶液。 |
步骤2.
步骤3.
|
___________________________
___________________________ |
(4)请计算,用635g水完全吸收“高温喷雾焙烧”产生的HCl气体 升(标准状况),即可得到36.5%的浓盐酸(相对原子质量 Cl 35.5 H 1)。
查看答案和解析>>
科目:高中化学 来源:2015届广东省惠州市高三第一次调研考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数,下列叙述正确的是
A.1mol?L-1 NaHCO3溶液中的Na+数为NA
B.常温时,2.24LCO2所含的氧原子数为0.2NA
C.5.6g Fe与足量稀盐酸反应,转移电子数为0.2NA
D.标准状况下,2.24L CCl4所含分子数为0.1NA
查看答案和解析>>
科目:高中化学 来源:2015届广东省广州市高三上学期第一次质量检测化学试卷(解析版) 题型:选择题
用下图装置(夹持、加热装置已略)进行实验,由②中现象,不能证实①中反应发生的是
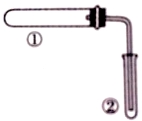
| ①中实验 | ②中现象 |
A | 铁粉与水蒸气加热 | 肥皂水冒泡 |
B | 加热NH4Cl和Ca(OH)2混合物 | 酚酞溶液变红 |
C | NaHCO3固体受热分解 | 澄清石灰水变浑浊 |
D | 石蜡油在碎瓷片上受热分解 | Br2的CCl4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源:2015届广东省广州市海珠区高三8月摸底考试理综化学试卷(解析版) 题型:填空题
(16分)二氧化钛(TiO2)又称钛白,工业上利用钛铁矿(主要成分FeTiO3,其中铁为正二价)为原料,采用硫酸法制得,其工艺流程如下图所示
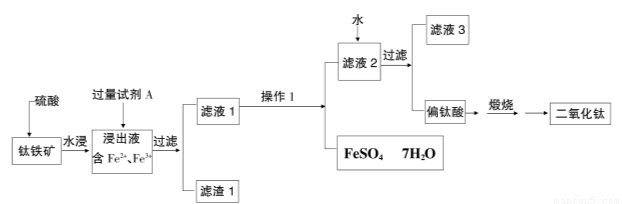
请回答:
(1)铁矿加入硫酸反应可制得硫酸氧钛,其反应的化学方程式为:
FeTiO3+ 2H2SO4=( )TiOSO4+( )+( );
(2)为了提高二氧化钛的纯度,需要除去浸出液中的Fe3+,则加入的试剂A为 ,需过量的原因是 。
(3)操作1是 。
(4)进行操作1时需将滤液1在70-75℃,压力8000Pa的条件下真空蒸发器中进行,其原因是为了防止 ,滤液2加水稀释使硫酸氧钛(TiOSO4)水解生成偏钛酸(TiO2·nH2O),请写出该水解反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2015届安徽省高三九月份化学月考试卷(解析版) 题型:选择题
下列说法中正确的是
 A.NO2、SO2、BF3分子中所有原子的最外层电子都满足了8e-稳定结构
A.NO2、SO2、BF3分子中所有原子的最外层电子都满足了8e-稳定结构
B.P4和CH4都是正四面体分子且键角都为109o28ˊ
C.NaCl晶体中与每个Na+距离相等且最近的Na+共有12个
D.原子间通过共价键而形成的晶体一定具有高的熔、沸点及硬度
查看答案和解析>>
科目:高中化学 来源:2015届安徽省六校教育研究会高三第一次联考化学试卷(解析版) 题型:填空题
C、O、Na、Al、S、Cl是常见的六种元素
(1)C元素位于元素周期表第 周期,第 族;C元素的一种同位素可以测定文物年代,这种同位素的符号为
(2)用“大于”“小于”或“等于”填空
离子半径 | 酸性 | 还原性 | 得电子能力 |
N3- Al3+ | H2SO4 HClO4 | O2- S2- | 35Cl 37Cl |
(3)① CaCO3和适量HCl溶液反应时,每产生4.4 g 气体(不考虑气体溶解),放热a kJ,则该反应的热化学方程式为 。
②上述反应至无气泡逸出后,取适量残留溶液,插入pH传感器并逐滴滴入碳酸钠溶液,测得pH变化曲线如图所示
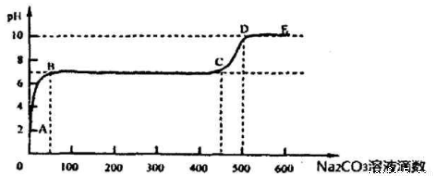
请用离子方程式表示B-C段发生的反应:
(4)氢气、氧气常用来作燃料电池,写出电解质为氢氧化钠溶液时负极上的电极方程式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com