
已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性;将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,需溶液的pH分 别为:6.4、6.4、3.7。现有含有FeCl2杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按下图所示步骤进行提纯:
别为:6.4、6.4、3.7。现有含有FeCl2杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按下图所示步骤进行提纯:
含杂质的水溶液Ⅰ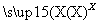 溶液Ⅱ
溶液Ⅱ 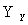
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案科目:高中化学 来源: 题型:
向一容积不变的密闭容器中充入一定量A和B,发生反应:xA(g)+2B(s)  yC(g) ΔH<0。在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如图所示。请回答下列问题:
yC(g) ΔH<0。在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如图所示。请回答下列问题:
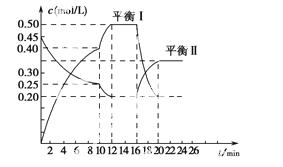
(1)用A的浓度变化表示该反应0~10 min内的平均反应速率v(A)=________。
(2)根据图示可确定x∶y=________。
(3)0~10 min容器内压强________(填“变大”、“不变”或“变小”)。
(4)推测第10 min引起曲线变化的反应条件可能是________;第16 min引起曲线变化的反应条件可能是________。
①减压 ②增大A的浓度 ③增大C的量 ④升温
⑤降温 ⑥加催化剂
(5)若平衡Ⅰ的平衡常数为K1,平衡Ⅱ的平衡常数为K2,则K1________K2(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
0.1 mol/L HF溶液的pH=2,则该溶液中有关浓度关系式不正确的是( )
A.c(H+)>c(F-) B.c(H+)>c(HF)
C.c(OH-)>c(HF) D.c(HF) >c(F-)
>c(F-)
查看答案和解析>>
科目:高中化学 来源: 题型:
两人用同一瓶盐酸滴定同一瓶NaOH溶液。甲将锥形瓶用NaOH待测液润洗后,使用水洗过的碱式滴定管取碱液于锥形瓶中 ;乙则用甲用过的滴定管取碱液于刚用蒸馏水洗过且存有
;乙则用甲用过的滴定管取碱液于刚用蒸馏水洗过且存有 蒸馏水的锥形瓶中,其他操作及读数均正确,你的判断是(
蒸馏水的锥形瓶中,其他操作及读数均正确,你的判断是(  )
)
A.甲操作有错
B.乙操作有错
C.甲测定数值一定比乙小
D.乙实际测得值较准确
查看答案和解析>>
科目:高中化学 来源: 题型:
不能用有关胶体的观点解释的现象是( )
A.在江河入海处易形成三角洲
B.在豆浆里加入盐卤做豆腐
C.在CaCl2溶液中滴入NaHCO3溶液看不到沉淀
D.同一钢笔同时使用不同牌号的墨水易发生堵塞
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与社会、生活密切相关。对下列现象或事实的解释正确的是( )
| 选项 | 现象或事实 | 解释 |
| A. | 用热的纯碱溶液洗去油污 | Na2CO3可直接与油污反应 |
| B. | 源白粉在空气中久置变质 | 漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
| C. | 施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用 | K2CO3与HN4Cl反应生成氨气会降低肥效 |
| D | FeCl3溶液可用于铜质印刷线路板制作 | FeCl3能从含Cu2+的溶液中置换出铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:
H2SO3是二元弱酸,NaHSO3溶液呈酸性。在0.1 mol·L-1 NaHSO3溶液
中,下列关系正确的是( )
A.c(HSO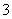 )>c(SO
)>c(SO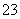 )>c(H2SO3)
)>c(H2SO3)
B.c(Na+)=c(HSO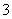 )+2c(SO
)+2c(SO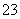 )+c(H2SO3)
)+c(H2SO3)
C.c(Na+)=c(HSO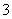 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
D.c(Na+)+c(H+)=c(HSO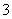 )+c(OH-)+c(SO
)+c(OH-)+c(SO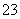 )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:I2+2S2O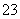 ===S4O
===S4O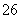 +2I-
+2I-
相关物质的溶度积常数见下表:
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl2 | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2·2H2O晶体,加入________,调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=________。过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2·2H2O晶体。
(2)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是____________________________(用化学方程式表示)。由CuCl2·2H2O晶体得到纯的无水CuCl2的合理方法是____________。
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.100 0 mol·L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20 .00 mL。
.00 mL。
①可选用_____作滴定指示剂,滴定终点的现象是__________。
②CuCl2溶液与KI反应的离子方程式为___________________。
③该试样中CuCl2·2H2O的质量百分数为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com