
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®ŅŅ“¼¼ČæÉŅŌ·¢Éś“ß»ÆŃõ»Æ·“Ó¦£¬ÓÖæÉŅŌ·¢Éśõ„»Æ·“Ó¦
B£®ÓĆäåĖ®æÉŅŌ¼ų±šŅŅ“¼”¢ŅŅĖįŗĶ±½
C£®ĢĒĄą”¢ÓĶÖ¬”¢µ°°×ÖŹČżĄąĪļÖŹ¶¼Ö»ŗ¬ÓŠC”¢H”¢OČżÖÖŌŖĖŲ
D£®C5H10OŹōÓŚČ©ĄąµÄĶ¬·ÖŅģ¹¹ĢåĪŖĮłÖÖ

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016Ń§ÄźÉ½¶«ŹŁ¹āĻÖ“śÖŠŃ§ø߶žÉĻ12ŌĀŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A£®0.1mol•L-1Na2CO3ČÜŅŗÖŠ£ŗc(OH-)=c(HCO3-)+c(H+)+c(H2CO3)
B£®0.1mol•L-1CH3COONaČÜŅŗÖŠ£ŗc(Na+)=c(CH3COO-)+c(OH-)
C£®CH3COONa”¢NaOHŗĶNa2CO3ČżÖÖČÜŅŗµÄpHĻąĶ¬£¬ŌņÅØ¶Č“óŠ”Ė³Šņ£ŗ
c(NaOH)£¼c(Na2CO3)£¼c(CH3COONa)
D£®Ļņ0.1mol•L-1CH3COOHČÜŅŗÖŠµĪ¼ÓNaOHČÜŅŗÖĮÖŠŠŌ£¬ČÜŅŗÖŠĄė×ÓÅØ¶ČµÄ¹ŲĻµ£ŗc(CH3COO-)£¾c(Na+)£¾c(OH-)=c(H+)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģ½ĖÕŹ”øßČżÉĻѧʌʌ֊²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ŃĒĀČĖįÄĘ£ØNaClO2£©Ö÷ŅŖÓĆÓŚĆŽ·Ä”¢ŌģÖ½ŅµµÄĘÆ°×¼Į£¬Ņ²ÓĆÓŚŹ³Ę·Ļū¶¾”¢Ė®“¦ĄķµČ”£ŅŃÖŖ¢ŁŃĒĀČĖįÄĘ£ØNaClO2£©ŹÜČČŅ×·Ö½ā”£
¢ŚNaClO2µÄČܽā¶ČĖęĪĀ¶ČÉżø߶ųŌö“ó£¬ŹŹµ±Ģõ¼žĻĀæɽį¾§Īö³öNaClO2”¤3H2O”£
¢Ū“æClO2Ņ×·Ö½ā±¬ÕØ£¬Ņ»°ćÓĆĻ”ÓŠĘųĢå»ņæÕĘųĻ”ŹĶµ½10%ŅŌĻĀ°²Č«”£
ŅŌĀČĖįÄʵČĪŖŌĮĻÖʱøŃĒĀČĖįÄĘµÄ¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ
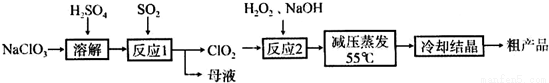
£Ø1£©”°·“Ó¦1”±ŠčŅŖ¹ÄČėæÕĘų£¬æÕĘųµÄ×÷ÓĆŹĒ_______________
£Ø2£©”°·“Ó¦2”±µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ_______________
£Ø3£©²ÉČ””°¼õŃ¹Õō·¢”±¶ų²»ÓĆ”°³£Ń¹Õō·¢”±£¬ŌŅņŹĒ_______________£»½į¾§ŗóŠčŅŖ¶Ō¾§ĢåĻ“µÓ£¬ĪŖĮĖ¼õÉŁĖšŹ§£¬æÉŅŌÓĆ_______Ļ“Ōč¾§Ģ唣
£Ø4£©“Ó”°ÄøŅŗ”±ÖŠæÉ»ŲŹÕµÄÖ÷ŅŖĪļÖŹŹĒ___________£»
£Ø5£©ŅŖµĆµ½“æµÄŃĒĀČĖįÄĘ¾§Ģå£ØNaClO2”¤3H2O£©£¬¶Ō“Ö²śĘ·µÄ±ŲŠė½ųŠŠµÄ²Ł×÷Ćū³Ę__________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģ½Ī÷Ź”øßČżÉĻѧʌʌ֊²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£Źż£¬ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ
A£®1molÅØĮņĖįŗĶ×ćĮæĶ·Ū·“Ó¦×ŖŅʵĵē×ÓŹżĪŖNA
B£®±ź×¼×“æöĻĀ£¬5.6LNOŗĶ5.6 LO2»ģŗĻŗóµÄ·Ö×Ó×ÜŹżĪŖĪŖ0.5NA
C£®0.1mol±½ŅŅĻ©ÖŠŗ¬ÓŠµÄĢ¼Ģ¼Ė«¼üµÄŹżÄæĪŖ0.1 NA
D£®½«NAøöNH3·Ö×ÓČÜÓŚ1LĖ®ÖŠµĆµ½1 mol•L-1µÄ°±Ė®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÖŲĒģŹŠøßČżÉĻѧʌµŚČż“ĪŌĀæ¼Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĶʶĻĢā
A”¢B”¢D”¢R”¢QĪåÖÖ¶ĢÖÜĘŚÖ÷×åŌŖĖŲ£¬ĘäŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĘäÖŠAŌ×ÓŗĖÄŚĪŽÖŠ×Ó£¬BÓėDĶ¬ÖÜĘŚ£¬RÓėQĶ¬ÖÜĘŚ£¬AÓėRĶ¬Ö÷×壬DÓėQĶ¬Ö÷×壬DŌŖĖŲµÄŌ×Ó×īĶā²ćµē×ÓŹżŹĒ“ĪĶā²ćµē×ÓŹżµÄČż±¶£¬BŌŖĖŲµÄ×īøßÕż¼ŪŗĶ×īµĶøŗ¼Ū“śŹżŗĶĪŖ2”£ĒėÓƶŌÓ¦µÄ»ÆѧÓĆÓļ»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©QŌŖĖŲĪ»ÓŚŌŖĖŲÖÜĘŚ±ķÖŠµŚ______ÖÜĘŚ_____×唣
£Ø2£©D”¢R”¢QČżÖÖŌŖĖŲŠĪ³ÉµÄ¼ņµ„Ąė×ӵİė¾¶Óɓ󵽊”µÄĖ³ŠņŹĒ________£ØÓĆĄė×Ó·ūŗűķŹ¾£©”£
£Ø3£©ÓÉA”¢BĮ½ÖÖŌŖĖŲŅŌŌ×ÓøöŹż±ČĪŖ5£ŗ1ŠĪ³ÉµÄĄė×Ó»ÆŗĻĪļX£¬XµÄµē×ÓŹ½ĪŖ_______”£
£Ø4£©ÓÉA”¢BŌŖĖŲŠĪ³ÉµÄA2B4æÉŅŌÓėO2”¢KOHČÜŅŗŠĪ³ÉŌµē³Ų£¬øĆŌµē³Ųøŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖ____”£
£Ø5£©ÓÉA”¢D”¢R”¢QĖÄÖÖŌŖĖŲŠĪ³ÉµÄ»ÆŗĻĪļY£ØRAQD3£©£ØŅŃÖŖA2QD3µÄKa1=1.2”Į10-2”¢Ka2=6.3”Į10-8£©£¬ŌņYČÜŅŗÖŠø÷Ąė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņĪŖ_______________£»ŹŅĪĀĻĀ£¬ĻņYČÜŅŗÖŠ¼ÓČėŅ»¶ØĮæµÄNaOH£¬Ź¹ČÜŅŗÖŠc(AQD3-)=c(QD32-)£¬Ōņ“ĖŹ±ČÜŅŗ³Ź______£ØĢī”°ĖįŠŌ”±”¢”°¼īŠŌ”±»ņ”°ÖŠŠŌ”±£©
£Ø6£©FeÓėDŌŖĖŲæÉŠĪ³ÉFe2D3”¢Fe3D4µČ»ÆŗĻĪļ”£Ļņ5.2g Fe2D3”¢Fe3D4”¢CuµÄ»ģŗĻÖŠ¼ÓČė0.5mol/LµÄĮņĖįČÜŅŗ140mLŹ±£¬¹ĢĢåĒ”ŗĆĶźČ«Čܽā£¬ĖłµĆČÜŅŗÖŠ²»ŗ¬Fe3+”£ČōÓĆ¹żĮæµÄCOŌŚøßĪĀĻĀ»¹ŌĻąĶ¬ÖŹĮæµÄŌ»ģŗĻĪļ£¬¹ĢĢå¼õÉŁµÄÖŹĮæĪŖ______g”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ°²»ÕŹ”øßŅ»ÉĻĘŚÖŠ²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
12 ml 0.1mol/LµÄŃĒĮņĖį(H2SO3)ČÜŅŗ£¬Ē”ŗĆøś20mlÅضČĪŖ0.02mol/LµÄÖŲøõĖį¼Ų£ØK2Cr2O7£©ČÜŅŗĶźČ«·“Ó¦£¬²śĪļÖ®Ņ»ĪŖH2SO4£¬ŌņŌŖĖŲøõ£ØCr£©ŌŚ»¹Ō²śĪļÖŠµÄ»ÆŗĻ¼ŪŹĒ£Ø £©
A£®+1 B£®+2 C£®+3 D£®+6
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ°²»ÕŹ”øßŅ»ÉĻĘŚÖŠ²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĪļÖŹ·ÖĄąµÄÕżČ·×éŗĻŹĒ£Ø £©
¼ī | Ėį | ŃĪ | ĖįŠŌŃõ»ÆĪļ | |
A | “æ¼ī | ŃĪĖį | ÉÕ¼ī | ¶žŃõ»ÆĮņ |
B | ÉÕ¼ī | ĮņĖį | Ź³ŃĪ | Ņ»Ńõ»ÆĢ¼ |
C | °±Ė® | “×Ėį | ŹÆ»ŅŹÆ | ¶žŃõ»ÆĢ¼ |
D | æĮŠŌ¼Ų | Ģ¼Ėį | µØ·Æ | ¶žŃõ»ÆĢ¼ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğÕć½Ź”øßŅ»ÉĻĘŚÖŠ²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŠšŹö“ķĪóµÄŹĒ
A£®13CŗĶ14CŹōÓŚĶ¬Ņ»ÖÖŌŖĖŲ£¬ĖüĆĒ»„ĪŖĶ¬Ī»ĖŲ
B£®1HŗĶ2HŹĒ²»Ķ¬µÄŗĖĖŲ£¬ĖüĆĒµÄÖŹ×ÓŹżĻąµČ
C£®14CŗĶ14NµÄÖŹĮæŹżĻąµČ£¬ĖüĆĒµÄÖŠ×ÓŹż²»µČ
D£®6LiŗĶ7LiµÄµē×ÓŹżĻąµČ£¬ÖŠ×ÓŹżŅ²ĻąµČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗÓ±±Ź”ø߶žÉĻ12ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĶʶĻĢā
A”¢B”¢C”¢D”¢E“ś±ķĪåÖÖ³£¼ūŌŖĖŲ£¬ĖüĆĒµÄŗĖµēŗÉŹżŅĄ“ĪŌö“ó”£ĘäÖŠŌŖĖŲEµÄ»łĢ¬3d¹ģµĄÉĻÓŠ2øöµē×Ó£¬AµÄ»łĢ¬Ō×ÓL²ćµē×ÓŹżŹĒK²ćµē×ÓŹżµÄ2±¶£¬ BŹĒµŲæĒÖŠŗ¬Įæ×ī¶ąµÄŌŖĖŲ£¬CŹĒ¶ĢÖÜĘŚÖŠ×ī»īĘĆµÄ½šŹōŌŖĖŲ£¬DÓėCæÉŠĪ³ÉCDŠĶĄė×Ó»ÆŗĻĪļ”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©EµÄ»łĢ¬Ō×Ó¼Ū²ćµē×ÓÅŲ¼Ź½ĪŖ_______________________________”£
£Ø2£©AB2·Ö×ÓÖŠ£¬AµÄŌÓ»ÆĄąŠĶĪŖ_______________________________”£
£Ø3£©AB2ŠĪ³ÉµÄ¾§ĢåµÄČŪµć________(Ģī”°“óÓŚ”±”¢”°Š”ÓŚ”±»ņ”°ĪŽ·ØÅŠ¶Ļ”±)CDŠĪ³ÉµÄ¾§ĢåµÄČŪµć£¬ŌŅņŹĒ_________________________”£
£Ø4£©EÓėBŠĪ³ÉµÄŅ»ÖÖ³ČŗģÉ«¾§Ģ徧°ū½į¹¹ČēĶ¼ĖłŹ¾£¬Ęä»ÆѧŹ½ĪŖ_______(ÓĆŌŖĖŲ·ūŗűķŹ¾)”£
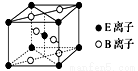
£Ø5£©ÓÉC”¢DĮ½ŌŖĖŲŠĪ³ÉµÄ»ÆŗĻĪļ×é³ÉµÄ¾§ĢåÖŠ£¬Ņõ”¢ŃōĄė×Ó¶¼¾ßÓŠ»ņ½üĖĘ¾ßÓŠĒņŠĶ¶Ō³Ę½į¹¹£¬ĖüĆĒ¶¼æÉŅŌæ“×öøÕŠŌŌ²Ēņ£¬²¢±Ė“Ė”°ĻąĒŠ”±”£ČēĶ¼ĖłŹ¾ĪŖC”¢DŠĪ³É»ÆŗĻĪļµÄ¾§°ū½į¹¹Ķ¼ŅŌ¼°¾§°ūµÄĘŹĆęĶ¼£ŗ
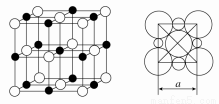
Čōa£½5.6”Į10£8 cm£¬ŌņøĆ¾§ĢåµÄĆܶČĪŖ________g”¤cm£3(¾«Č·µ½Š”Źżµćŗó1Ī»)”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com