
�������ƣ�Na2FeO4�����к�ǿ�������ԣ���һ�ֱ��������õľ�ˮ����������ҵ�Ͽ���ͨ�����������������Ʊ��������ƣ������������£��ش��������⣺
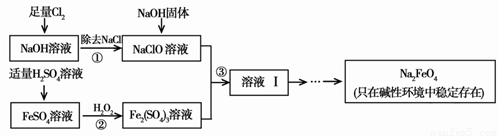
��1����������ˮ����������Ϊ������ˮ������________������ǿ�������ԣ���ɱ��������
��2������ڷ�Ӧ�����ӷ���ʽ�� ��
��3������Һ���з����Na2FeO4���и���ƷNa2SO4 ��NaCl��������з�Ӧ�����ӷ���ʽΪ ��
��4����һ������Na2FeO4Ͷ�뵽pH��ͬ����ˮ�У���ˮ������ɷ־���ͬ������Һ��Na2FeO4Ũ�ȱ仯��ͼ���ߢ���ʾ�����Ʋ�����II������I��Ӧ����ˮpH________����ߡ��͡�����
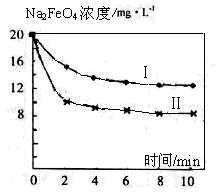
��5��ͨ�������֪Na2FeO4������Ч�ʣ��Ե�λ�����õ��ĵ�������ʾ��Լ��������_____��
��1���������HClO ��2��2Fe2+ + H2O2 + 2H+ = 2Fe3+ + 2H2O
��3��2Fe3+ + 3ClO- + 10OH- = 2FeO42- + 3Cl- + 5H2O ��4���� ��5��0.64��
��������
�����������1��������ˮ�з�����Ӧ��Cl2+H2O=HCl+HClO. HclO��ǿ�������ԣ��ܶ�ˮɱ������������2��H2O2��ǿ�������ԣ������������°�Fe2+������Fe3+������������ԭΪH2O������ڷ�Ӧ�����ӷ���ʽ��2Fe2+ + H2O2 + 2H+ = 2Fe3+ + 2H2O����3��ClO-���ڼ��������°�Fe3+������FeO42-������������ΪCl-��������з�Ӧ�����ӷ���ʽΪ2Fe3+ + 3ClO- + 10OH- = 2FeO42- + 3Cl- + 5H2O ����4��FeO42-���������������������ȼ���������ǿ��Ũ�ȱ仯����������II������I��Ӧ����ˮpHС��������ǿ����5��Na2FeO4������Ч���ǣ�3NA��166������������Ч���ǣ�2NA��71.����Na2FeO4������Ч������������Ч��֮��Ϊ����3NA��166������2NA��71��=0.64..
���㣺���龻ˮ�������������ƣ�Na2FeO4�����Ʒ�������Ч�ʼ���Ӧ�Ļ�ѧ��Ӧԭ����


 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
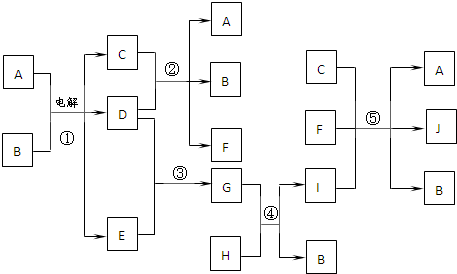
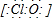
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
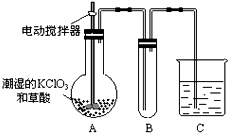 �ö������ȣ�ClO2�����������ƣ�Na2FeO4Ħ������Ϊ166g?mol-1�������;�ˮ�������ͳ�ľ�ˮ��Cl2�Ե�ˮ���������dz�������ˮ�����¼�����ClO2��Na2FeO4��ˮ���������зֱ𱻻�ԭΪCl-��Fe3+��
�ö������ȣ�ClO2�����������ƣ�Na2FeO4Ħ������Ϊ166g?mol-1�������;�ˮ�������ͳ�ľ�ˮ��Cl2�Ե�ˮ���������dz�������ˮ�����¼�����ClO2��Na2FeO4��ˮ���������зֱ𱻻�ԭΪCl-��Fe3+���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| A����Ӧ��Na2O2�������� |
| B��Fe2O3����ͨ����˿��������ȼ���Ƶ� |
| C������1 mol Na2FeO4����6 mol����ת�� |
| D����Na2FeO4��FeΪ+4�ۣ�����ǿ�����ԣ�������ɱ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com