
”¾ĢāÄæ”æŅŃÖŖ·“Ó¦£ŗ2SO2£Øg£©+O2£Øg£©2SO3£Øg£©”÷H£¼0£®Ä³ĪĀ¶ČĻĀ£¬½«2mol SO2ŗĶ1mol O2ÖĆÓŚ10LĆܱÕČŻĘ÷ÖŠ£¬·“Ó¦“ļĘ½ŗāŗó£¬SO2µÄĘ½ŗā×Ŗ»ÆĀŹ£Ø¦Į£©ÓėĢåĻµ×ÜŃ¹Ēæ£Øp£©µÄ¹ŲĻµČēĶ¼¼×ĖłŹ¾£®ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £© 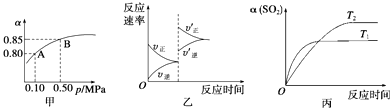
A.ÓÉĶ¼¼×ÖŖ£¬AµćSO2µÄĘ½ŗāÅضČĪŖ0.4 mol/L
B.ÓÉĶ¼¼×ÖŖ£¬BµćSO2”¢O2”¢SO3µÄĘ½ŗāÅضČÖ®±ČĪŖ2£ŗ1£ŗ2
C.“ļĘ½ŗāŗó£¬ĖõŠ”ČŻĘ÷ČŻ»ż£¬Ōņ·“Ó¦ĖŁĀŹ±ä»ÆĶ¼ĻńæÉŅŌÓĆĶ¼ŅŅ±ķŹ¾
D.Ń¹ĒæĪŖ0.50 MPaŹ±²»Ķ¬ĪĀ¶ČĻĀSO2×Ŗ»ÆĀŹÓėĪĀ¶Č¹ŲĻµČē±ūĶ¼£¬ŌņT2£¾T1
”¾“š°ø”æC
”¾½āĪö”æ½ā£ŗA”¢¶žŃõ»ÆĮņĘšŹ¼ÅضČĪŖ ![]() =0.2mol/L£¬Óɼ×Ķ¼æÉÖŖAµćSO2µÄ×Ŗ»ÆĀŹĪŖ0.8£¬ĖłŅŌ”÷c£ØSO2£©=0.8”Į0.2mol/L=0.16mol/L£¬¹Ź¶žŃõ»ÆĮņµÄĘ½ŗāÅضČĪŖ0.2mol/L©0.16mol/L=0.04mol/L£¬¹ŹA“ķĪó£» B”¢Óɼ×Ķ¼æÉÖŖBµćSO2µÄ×Ŗ»ÆĀŹĪŖ0.85£¬ĖłŅŌ”÷c£ØSO2£©=0.85”Į0.2mol/L=0.17mol/L£¬Ōņ£ŗ
=0.2mol/L£¬Óɼ×Ķ¼æÉÖŖAµćSO2µÄ×Ŗ»ÆĀŹĪŖ0.8£¬ĖłŅŌ”÷c£ØSO2£©=0.8”Į0.2mol/L=0.16mol/L£¬¹Ź¶žŃõ»ÆĮņµÄĘ½ŗāÅضČĪŖ0.2mol/L©0.16mol/L=0.04mol/L£¬¹ŹA“ķĪó£» B”¢Óɼ×Ķ¼æÉÖŖBµćSO2µÄ×Ŗ»ÆĀŹĪŖ0.85£¬ĖłŅŌ”÷c£ØSO2£©=0.85”Į0.2mol/L=0.17mol/L£¬Ōņ£ŗ
2SO2£Øg£©+ | O2£Øg£© | 2SO3£Øg£© | ||
æŖŹ¼£Ømol/L£©£ŗ | 0.2 | 0.1 | 0 | |
±ä»Æ£Ømol/L£©£ŗ | 0.17 | 0.085 | 0.17 | |
Ę½ŗā£Ømol/L£©£ŗ | 0.03 | 0.015 | 0.17 |
ĖłŅŌBµćSO2”¢O2”¢SO3µÄĘ½ŗāÅضČÖ®±ČĪŖ0.03£ŗ0.015£ŗ0.17=6£ŗ3£ŗ34£¬¹ŹB“ķĪó£»
C”¢“ļĘ½ŗāŗó£¬ĖõŠ”ČŻĘ÷ČŻ»ż£¬·“Ó¦»ģŗĻĪļµÄÅØ¶Č¶¼Ōö“ó£¬Õż”¢Äę·“Ó¦ĖŁĀŹ¶¼Ōö“ó£¬ĢåĻµŃ¹ĒæŌö“ó£¬Ę½ŗāĻņĢå»ż¼õŠ”µÄ·“Ó¦ŅĘ¶Æ£¬¼“Ę½ŗāĻņÕż·“Ó¦ŅĘ¶Æ£¬¹ŹV£ØÕż£©£¾V£ØÄę£©£¬¹ŹCÕżČ·£»
D”¢Óɵ½“ļĘ½ŗāµÄŹ±¼äæÉÖŖ£¬ĪĀ¶ČĪŖT1 £¬ Ļȵ½“ļĘ½ŗā£¬·“Ó¦ĖŁĀŹæģ£¬ĪĀ¶ČŌ½øß·“Ó¦ĖŁĀŹŌ½æģ£¬¹ŹT2£¼T1 £¬ ¹ŹD“ķĪó£»
¹ŹŃ”C£®


 Č«Óųå“Ģ100·ÖĻµĮŠ“š°ø
Č«Óųå“Ģ100·ÖĻµĮŠ“š°ø Ó¢²Åµć½ņĻµĮŠ“š°ø
Ó¢²Åµć½ņĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓÉW”¢X”¢Y”¢ZĖÄÖÖ½šŹō°“ĻĀĮŠ×°ÖĆ½ųŠŠŹµŃ飮ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
×°ÖĆ |
|
|
|
ĻÖĻó | ½šŹōW²»¶ĻČܽā | YµÄÖŹĮæŌö¼Ó | WÉĻÓŠĘųĢå·¢Éś |
A.×°ÖĆ¼×ÖŠW×÷Ōµē³Ųøŗ¼«
B.×°ÖĆŅŅÖŠYµē¼«ÉĻµÄ·“Ó¦Ź½ĪŖCu2++2e©=Cu
C.×°ÖƱūÖŠČÜŅŗµÄpH¼õŠ”
D.ĖÄÖÖ½šŹōµÄ»ī¶ÆŠŌĒæČõĖ³ŠņĪŖZ£¾W£¾X£¾Y
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¹¹½ØŗĶŠ³Éē»įµÄÄŚČŻÖ®Ņ»ŹĒČĖĄąÓė»·¾³µÄŗĶŠ³·¢Õ¹£¬¶ų”°ĀĢÉ«»Æѧ”±µÄÄŚČŻŹĒÖø“Ó¼¼Źõ¾¼ĆÉĻÉč¼ĘæÉŠŠµÄ»Æѧ·“Ó¦£¬¾”æÉÄܼõÉŁ¶Ō»·¾³µÄø±×÷ÓĆ£¬ĻĀĮŠ»Æѧ·“Ó¦²»·ūŗĻ”°ĀĢÉ«»Æѧ”±øÅÄīµÄŹĒ( )
A.Ļū³żĮņĖį³§Ī²ĘųÖŠµÄSO2£ŗSO2£«2NH3£«H2O===(NH4)2SO3
B.Ļū³żĻõĖį¹¤ŅµĪ²ĘųµÄµŖŃõ»ÆĪļµÄĪŪČ¾£ŗNO£«NO2£«2NaOH===2NaNO2£«H2O
C.ÖĘCuSO4£ŗCu£«2H2SO4(ÅØ) ![]() CuSO4£«SO2”ü£«2H2O
CuSO4£«SO2”ü£«2H2O
D.ÖĘCuSO4£ŗ2Cu£«O2£«2H2SO4 ![]() 2CuSO4£«2H2O
2CuSO4£«2H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹµĻÖĻĀĮŠ×Ŗ»ÆµÄ·“Ó¦·½³ĢŹ½ÖŠ£¬ÕżČ·µÄŹĒ£Ø £©
A.H2SO3”śH2SO4£ŗ2H2SO3+O2=2H2SO4
B.Fe”śFe3+£ŗ2Fe+6H+=2Fe3++3H2”ü
C.Br©”śBr2£ŗ2Br©+I2=Br2+2I©
D.Cu”śCuSO4£ŗCu+2H2SO4£ØĻ”£©=CuSO4+SO2”ü+2H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŗĻ½šŹĒ³£ÓĆµÄ²ÄĮĻ£®ĻĀĮŠ²śĘ·²»ŹōÓŚŗĻ½šÖĘĘ·µÄŹĒ£Ø £©
A.Ģś¹ų
B.½šŹōĆÅ“°
C.²»ŠāøÖ²Ķ¾ß
D.Ė®ŅųĪĀ¶Č¼Ę
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ( )
A.ŅŅĻ©ŗĶ¾ŪŅŅĻ©µÄŠŌÖŹ²»Ķ¬
B.¾ŪŅŅĻ©ŹĒÓÉ”ŖCH2”ŖCH2”Ŗ·Ö×Ó×é³ÉµÄ»ÆŗĻĪļ£¬¼ÓČČÖĮijŅ»ĪĀ¶ČŌņæÉĶźČ«ČŪ»Æ
C.Ķ¬ÖŹĮæµÄŅŅĻ©ŗĶ¾ŪŅŅĻ©ĶźČ«Č¼ÉÕŗóÉś³ÉµÄCO2µÄÖŹĮæĻąµČ
D.ŅŅĻ©ŗĶ¾ŪŅŅĻ©µÄ×ī¼ņŹ½ĻąĶ¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĢģČ»Ęų”¢ÕÓĘųµÄÖ÷ŅŖ³É·Ö_________£ØĢī·Ö×ÓŹ½£©£¬øĆĘųĢå·Ö×ÓµÄæռ乹ŠĶŹĒ___________½į¹¹”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ±ä»Æ»ņÓ¦ÓĆÖŠ£¬Óė·Ö×Ó¼ä×÷ÓĆĮ¦ÓŠ¹ŲµÄŹĒ( )
A. ĀČ»ÆÄĘ¾§ĢåČÜÓŚĖ®B. ĻõĖį¼Ų¾§ĢåµÄČŚ»Æ”¢ĄäČ“
C. “ĪĀČĖįÓĆӌɱ¾śĻū¶¾D. ĻÄĢģĀķĀ·Č÷Ė®½µĪĀ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij³§µÄĖįŠŌ¹¤Ņµ·ĻĖ®ÖŠŗ¬ÓŠŅ»¶ØĮæµÄFe3£«”¢Cu2£«”¢Au3£«µČĄė×Ó”£ÓŠČĖÉč¼ĘĮĖĶ¼ÖŠµÄ¹¤ŅÕĮ÷³Ģ£¬ĄūÓĆ³£ÓƵÄĖį”¢¼īŗĶ¹¤ŅµÉś²śÖŠµÄ·ĻĢśŠ¼£¬“Ó·ĻĖ®ÖŠ»ŲŹÕ½š£¬²¢Éś²śŅ»¶ØĮæµÄĢśŗģŗĶŃõ»ÆĶ”£
ĢīŠ“ĻĀĆęæÕ°×”£
£Ø1£©Ķ¼ÖŠ±źŗÅ“¦Šč¼ÓČėµÄĻąÓ¦ĪļÖŹ·Ö±šŹĒ¢Ł”¢¢Ś”¢¢Ū”¢¢Ü”¢¢Ż£»
£Ø2£©Š“³ö¢Ł“¦·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½£»
Š“³ö¢Ū“¦·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½£»
£Ø3£©ĢśŗģµÄ»ÆѧŹ½ĪŖ£»·Ö±šŠ“³öĢśŗģŗĶŃõ»ÆĶŌŚ¹¤ŅµÉĻµÄŅ»ÖÖÖ÷ŅŖÓĆĶ¾£ŗĢśŗģ£»Ńõ»ÆĶ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com