
| A. | 面粉-淀粉 | B. | 牛肉-蛋白质 | C. | 桔子-维生素 | D. | 梅子蜜饯-防腐剂 |
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源: 题型:解答题
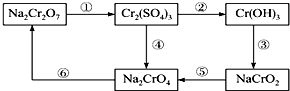
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某温度下,任何电解质的水溶液中:pC(H+)+pC(OH-)=14 | |
| B. | 某温度下,AB难溶性离子化合物的Ksp=1.0×10-10,其饱和溶液中:pC(A+)+pC(B-)=10 | |
| C. | 0.01mol/L的盐酸滴定某浓度的氨水溶液,滴定终时:pC(Cl-)>pC(NH4+)>pC(H+)>pC(OH-) | |
| D. | 0.01mol/L的醋酸钠溶液中:pC(Na+)+pC(H+)=pC(OH)-+pC(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
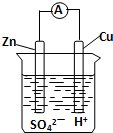
| A. | 锌电极上发生还原反应 | |
| B. | 铜电极上发生氧化反应 | |
| C. | 锌片和铜片上都有氧气产生 | |
| D. | 原电池工作一段时间后溶液的c(H+)减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝酸浓度越大消耗的硝酸越少,产生的有毒气体也越少 | |
| B. | 反应中转移的电子总数稀硝酸少 | |
| C. | 试管内壁上的铜用浓硝酸除好,因反应速率快 | |
| D. | 两者用排水法收集的气体的体积相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
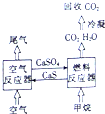 我国的能源主要来源于燃煤,煤燃烧产生的烟气直接排放会引起严重的环境问题.将烟气通过石灰石浆液的脱硫装置可以除去85%~90%的SO2,且最终会生成硫酸钙,将硫酸钙与甲烷通过循环燃烧装置的燃料反应器进行反应,生产出几乎不含杂质的二氧化碳,减少碳排放,其装置如图所示.
我国的能源主要来源于燃煤,煤燃烧产生的烟气直接排放会引起严重的环境问题.将烟气通过石灰石浆液的脱硫装置可以除去85%~90%的SO2,且最终会生成硫酸钙,将硫酸钙与甲烷通过循环燃烧装置的燃料反应器进行反应,生产出几乎不含杂质的二氧化碳,减少碳排放,其装置如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
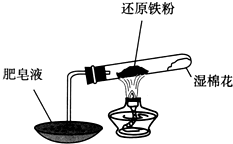
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末放入试管1中,加入盐酸,微热 | 黑色粉末逐渐溶解,溶液呈浅绿色;有少量气泡产生 |
| ② | 向试管1中滴加几滴KSCN溶液,振荡 | 溶液没有出现血红色 |
| A. | 试管内的固体一定含有铁粉 | |
| B. | 试管内的固体一定不含有Fe3O4 | |
| C. | 不能确定试管内的固体一定含有FeO | |
| D. | 可通过将试管内固体彻底还原,分析其质量减小的方法来确定是否含有Fe3O4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com