
【题目】原电池的应用极为广泛。利用如下图所示原电池可测量空气中Cl2的含量,其中电解质是Ag+可以自由移动的固体物质,下列分析正确的是
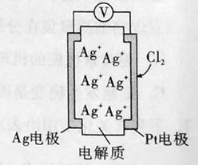
A.电流经外电路从Ag流向Pt电极
B.电池工作时,电解质中Ag+数目增多
C.正极反应:Cl2+2e-=2Cl-
D.空气中c(Cl2)越大,Ag极消耗速率越快
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】【化学——选修5:有机化学基础】
高分子化合物H的合成路线如下图所示:

(1)A的名称是 ,由A生成B的反应类型是 。
(2)C的结构简式为 ,F中官能团的名称为 。
(3)写出由E生成M的化学方程式: 。
(4)在催化剂存在下,D、G按物质的量之比为1:1发生加聚反应的化学方程式为 。
(5)Q是M的一种同系物,相对分子质量比M大14,Q有多种同分异构体,则符合下列条件的同分异构体共有 种。
①能与金属钠发生置换反应;②能发生银镜反应。写出其中核磁共振氢谱有4组峰的一种同分异构体的结构简式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化铈(CeO2)是一种重要的稀土氧化物。以氟碳铈矿(主要含CeFCO3)为原料制备CeO2的一种工艺流程如下:
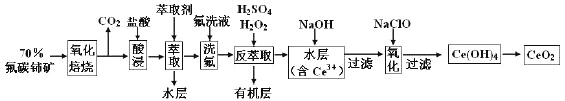
已知:①Ce4+既能与F-结合成[CeFx](4-x)+,也能与SO42-结合成[CeSO4]2+;
②在硫酸体系中Ce4+能被萃取剂[(HA)2]萃取,而Ce3+不能。
回答下列问题:
(1)“氧化焙烧”前需将矿石粉碎成细颗粒,其目的是__________________________。
(2)“酸浸”中会产生大量黄绿色气体,写出CeO2与盐酸反应的离子方程式:_________________________________;为避免产生上述污染,请提出一种解决方案:________。
(3)“萃取”时存在反应:Ce4++n(HA)2 ![]() Ce·(H2n-4A2n)+4H+。实验室中萃取时用到的主要玻璃仪器名称为___________; ____________________________________________________________。
Ce·(H2n-4A2n)+4H+。实验室中萃取时用到的主要玻璃仪器名称为___________; ____________________________________________________________。
(4)“反萃取”中,在稀硫酸和H2O2的作用下CeO2转化为Ce3+,H2O2在该反应中作_________(填“催化剂”、“氧化剂”或“还原剂”),每有1mol H2O2参加反应,转移电子的物质的量为________________。
(5)“氧化”步骤的化学方程式为________________________________。
(6)取上述流程中得到的CeO2产品0.4500g,加硫酸溶解后,用0.1000mol/LFeSO4标准溶液滴定至终点时(铈被还原为Ce3+,其它杂质均不反应),消耗25.00mL标准溶液。该产品中CeO2的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的NaOH溶液时,造成实验结果偏低的原因可能是 ( )
A. 容量瓶中原有少量蒸馏水
B. 称量药品时间过长
C. 定容时俯视液面
D. 洗涤烧杯和玻棒的溶液转入容量瓶中;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:
C(金刚石,s)+O2(g)===CO2(g) ΔH1
C(石墨,s)+O2(g)===CO2(g) ΔH2
C(石墨,s)===C(金刚石,s) ΔH3=+1.9 kJ·mol-1
下列说法正确的是( )
A.石墨转化成金刚石的反应是吸热反应
B.金刚石比石墨稳定
C.ΔH3=ΔH1-ΔH2
D.ΔH1>ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式2H2(g)+O2(g)===2H2O(l) ΔH1<0,则关于2H2O(l)===2H2(g)+O2(g) ΔH2的说法不正确的是( )
A.热化学方程式中的化学计量数只表示分子数
B.该反应的ΔH2应大于零
C.该反应的ΔH2=-ΔH1
D.该反应可表示36 g液态水完全分解生成气态氢气和氧气的热效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa、25℃时,16 gN2H4在氧气中完全燃烧生成氮气,放出热量312 kJ。N2H4完全燃烧反应的热化学方程式是 。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时:正极的电极反应式是 。负极的电极反应方程式是 。
(3)下图是一个电化学过程示意图。

① 锌片上发生的电极反应方程式是 。
② 假设使用肼—空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上消耗标准状况下的空气 L(假设空气中氧气体积含量为20%)
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液。该反应的离子方程式是 。
(5)将0.3 mol AgNO3、0.4 mol Cu(NO3)2和0.1mol KCl溶于水配成100 mL溶液,用惰性电极电解一段时间后,当阴极生成0.1mol气体时,此时,另一极上的气体体积(标准状况)为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在稀硫酸中加入铜粉,铜粉不溶,再加入下列物质:①FeCl3;②Fe2O3;③Cu(NO3)2;④KCl,铜粉溶解的是( )
A.只有①或② B.只有①或②或④
C.只有①或②或③ D.上述任意一种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com