
| A.推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应 |
| B.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” |
| C.废电池需回收,主要是要利用电池外壳的金属材料 |
| D.升高温度可降低活化能 |
 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源:不详 题型:单选题
| | 金属 | 存在形式 | 冶炼方法 |
| A | 金 | 游离态 | 金子比沙子密度大,利用水洗法直接分离 |
| B | 银 | 化合态 | 银的金属性弱,用加热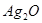 的方法冶炼 的方法冶炼 |
| C | 铁 | 化合态 | 铝的金属性比铁强,可用铝热法炼铁 |
| D | 钠 | 化合态 | 钠的金属性强,一般还原剂很难将其还原出来,所以用电解饱和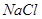 溶液方法冶炼 溶液方法冶炼 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氯碱工业中阳极得到氢氧化钠和氢气 |
| B.电镀铜时,电镀液中c(Cu2+)基本保持不变 |
| C.合成氨中采取及时分离液态氨来提高反应速率 |
| D.海水中含有钾元素,只需经过物理变化就可以得到钾单质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.制钛:用金属钠置换氯化钛(TiCl4)溶液中的钛 |
| B.炼铁:用焦炭和空气反应产生的CO在高温下还原铁矿石中的铁 |
| C.制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液 |
| D.炼铜:用黄铜矿(主要成分为CuFeS2)直接电解精炼得到纯度为99.9%的铜 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
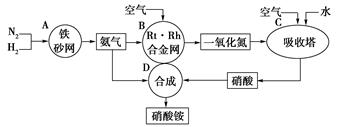
 (1)吸收塔C中通人空气的目的是
(1)吸收塔C中通人空气的目的是  2NH3(g);△H=-92kJ/mol。为提高氢气的转化率,宜采取的措施有 。(填字母)
2NH3(g);△H=-92kJ/mol。为提高氢气的转化率,宜采取的措施有 。(填字母)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用潮汐发电,将化学能转化为电能 | B.不需富集,直接提取海水中的溴 |
| C.用海水中的NaCl制取烧碱和纯碱 | D.只需使海水中的碘升华就能得到碘单质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
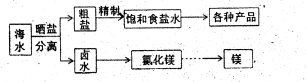
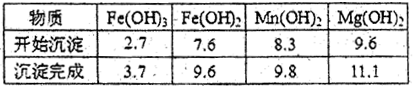
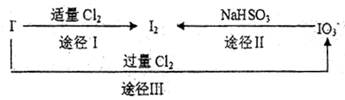
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
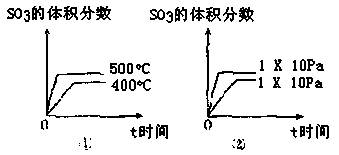
| A.H2O | B.稀H2SO4 |
| C.98.3%H2SO4 | D.NH3·H2O溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com