
|
为了确定某物质是否变质,所选试剂(括号内物质)不能达到实验目的的是 | |
| [ ] | |
A. |
FeSO4是否被氧化(KSCN) |
B. |
K2SO3是否被氧化(BaCl2) |
C. |
KI是否被氧化(淀粉溶液) |
D. |
漂粉精是否被变质(稀盐酸) |
 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:
| 实验方法 | 实验现象 | 结论 |
| 在溶液中加入KSCN溶液 | 溶液变红色 溶液变红色 . |
固体物质中有FeCl3 |
| 在酸性KMnO4溶液中加入少量A | KMnO4溶液颜色无明显变化 | 固体物质中不含 FeCl2 FeCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 实验方法 | 实验现象 | 结论 |
| 在溶液中加入KSCN溶液 | 溶液变血红色 溶液变血红色 |
固体物质中有FeCl3 |
| 在酸性KMnO4溶液中加入少量A | KMnO4溶液颜色无明显变化 | 固体物质中不含 FeCl2 FeCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源:学习周报 化学 人教课标高一版(必修1) 2009-2010学年 第16期 总第172期 人教课标版 题型:058
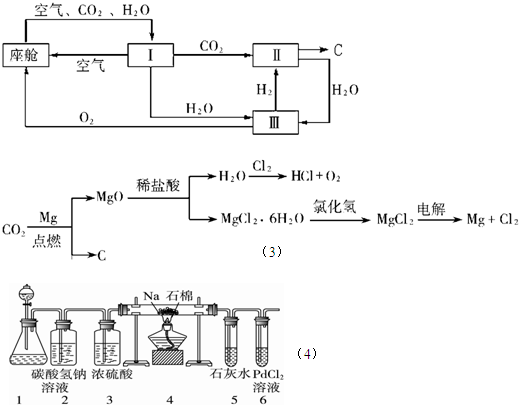
已知亚硫酸钠与硫酸反应可以生成二氧化硫.某课外兴趣小组为了探究某白色固体
M的成分,可能含Al粉、Na2SO3、Na2SO4、Na2CO3中的一种或多种,设计了如图所示的装置进行实验.
倾斜
A,使稀硫酸(足量)与固体M充分反应,待反应停止后,B中溶液紫红色变浅并增重,C中液体也增重.反应结束后进入量气管的气体体积为V mL.回答下列问题:(1)固体M中一定含有的物质是________(填化学式).
(2)写出C中发生反应的离子方程式:________________.
(3)量气管中的气体为________,理由是________________.
(4)固体M中不能确定是否存在的物质是________(填化学式).如果想进一步确定该物质是否存在,有同学提出实验完毕后,拆下仪器A,向其中加入BaCl2溶液,观察是否生成沉淀即可.你认为此方案可行吗?________(填“可行”或“不可行”),理由是________.如果不可行,请你提出改进方案:________(如答“可行”,此空不填).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com