
【题目】在两个容积相同的容器中,一个盛有C3H8气体,另—个盛有N2O和CO2的混合气体。在同温同压下,两容器内的气体一定具有相同的①分子数②密度③质量④质子数⑤原子数
A. ①②③ B. ①②⑤ C. ③④⑤ D. ①④⑤
科目:高中化学 来源: 题型:
【题目】1molX气体跟amolY气体在体积可变的密闭容器中发生如下反应:X(g)+aY(g)![]() bZ(g).反应达到平衡后,测得X的转化率为25%.而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的5/6,则a和b数值可能是( )
bZ(g).反应达到平衡后,测得X的转化率为25%.而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的5/6,则a和b数值可能是( )
A. a=1,b=2 B. a=1,b=3
C. a=2,b=3 D. a=2,b=1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G均为短周期元素,原子序数依次递增。A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的主族元素。请回答下列问题:
(1)C在元素周期表中的位置为______________,G的原子结构示意图是___________。
(2)D与E按原子个数比1:1形成化合物甲,其电子式为____________________,所含化学键类型为___________________。向甲中滴加足量水时发生反应的化学方程式是___________________________。
(3)E、F、G形成的简单离子,半径由大到小顺序是____________。(用离子符号表示)
(4)用BA4、D2和EDA的水溶液组成燃料电池,电极材料为多孔惰性金属电极。在a极通入BA4气体,b极通入D2气体,则b极是该电池的_____极,负极的电极反应式为_______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组选用以下装置(夹持装置省略,装置可重复选用)进行氯化亚铁与氧气反应的探究。已知氯化亚铁的熔点674℃、沸点1023℃;三氯化铁在300℃以上易升华,易溶于水并且有强烈的吸水性。在500℃条件下氯化亚铁与氧气可能发生多种反应,反应之一为:12FeCl2 +3O2![]() 2Fe2O3 +8FeCl3。回答下列问题:
2Fe2O3 +8FeCl3。回答下列问题:
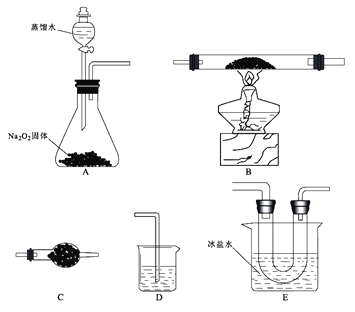
(1)仪器C的名称____________,连接好装置后,加入药品前的操作为___________________。
(2)E装置的作用是______________。
(3)反应过程发现,装置B中除生成红棕色固体外,还观察到黄绿色气体,生成该气体的化学方程式为_____________________________。
(4)待B中充分反应后,停止加热,仍继续通入氧气直至反应管冷却。则停止加热前是否需要先将D中导管口移出水面,为什么?
_____________________________。
(5)设计实验:
①利用E装置U形管里的固体验证Fe(OH)3是弱碱:___________________。(简明扼要写方法)
②利用E装置U形管里的固体,配成溶液,制得某种胶体,写出制备该胶体的化学方程式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与淀粉相关的物质间转化关系如下图所示。其中B的分子中含有一个甲基,B与羧酸和醇均能发生酯化反应;C的催化氧化产物既是合成酚醛树脂的原料之一,又是常见的居室污染物;E能使Br2的CCl4溶液褪色。

(1)B的结构简式是_____________________________。
(2)E→F的化学方程式是___________________________。
(3)某同学欲验证淀粉完全水解的产物A,进行如下实验操作:①在试管中加入少量淀粉溶液;②加热3~4 min;③加入少量新制的Cu(OH)2悬浊液;④加入少量稀硫酸;⑤加热;⑥待冷却后,滴加NaOH溶液至溶液呈碱性。则以上操作步骤正确的顺序是(填选项序号)_____________。
A.①②④⑤③⑥ | B.①④②③⑤⑥ | C.①④②⑥③⑤ | D.①⑤③④⑥② |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)X、Y、W、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知X的一种核素的质量数为18,中子数为10,Y和Ne原子的核外电子总数相差1;W的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最大。

(1)W位于元素周期表中第 周期第 族画出X的阴离子的结构示意图 。
(2)Z的氢化物和溴化氢相比,较稳定的是 (写化学式);Z的氢化物与氟化氢相比,沸点较高的是 (写化学式)。
(3)Y的金属性与Mg的金属性相比, (写化学式)的金属性强,请用实验证明它们金属性的相对强弱: 。
(4)写出Y的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物发生反应的化学反应方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨在工农业生产中应用广泛。
(1)根据下图写出合成氨的热化学方程式是________________________。

(2)将1 mol N2(g)和3 mol H2(g)放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量___________(填“大于”、“等于”或“小于”)92.2 kJ,原因是______________;若加入催化剂,ΔH________(填“变大”、“不变”或“变小”)。
(3)已知分别破坏1 mol N≡N键、1 mol H-H键时需要吸收的能量为946 kJ、436 kJ,则破坏1 mol N—H键需要吸收的能量为________kJ。
(4)N2H4可视为NH3分子中的H被-NH2取代的产物。发射卫星时以N2H4(g)为燃料、NO2为氧化剂,二者反应生成N2和H2O(g)。
已知:N2(g)+2O2(g)==2NO2(g) ΔH1=+67.7 kJ·mol-1
N2H4(g)+O2(g)==N2(g)+2H2O(g) ΔH2=-534 kJ·mol-1
则1 mol N2H4与NO2完全反应的热化学方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2016·江苏化学,13,4分)根据下列实验操作和现象所得到的结论正确的是(双选)( )
选项 | 实验操作和现象 | 结论 |
A | 室温下,向苯酚钠溶液中通入足量CO2,溶液变浑浊。 | 碳酸的酸性比苯酚的强 |
B | 室温下,向浓度均为0.1 mol·L-1的BaCl2和CaCl2混合溶液中滴加Na2SO4溶液,出现白色沉淀。 | Ksp(BaSO4)<Ksp(CaSO4) |
C | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色。 | Fe3+的氧化性比I2的强 |
D | 室温下,用pH试纸测得:0.1 mol·L-1Na2SO3溶液的pH约为10;0.1mol·L-1NaHSO3溶液的pH约为5。 | HSO |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)![]() U原子核的中子数与质子数之差为____________。
U原子核的中子数与质子数之差为____________。
(2)为了便于理解物质的组成,Fe3O4可改写为FeO· Fe2O3 则 Pb3O4可改写为:__________。
(3)O3、NH4NO3、K2O2、N2H4四种物质中,既有离子键又有非极性键的是_____________。
(4)金刚石、NaOH、干冰三物质中,熔化时需要破坏共价键的是________。
(5)氯化铝的物理性质非常特殊,如:氯化铝的熔点为190 ℃(2.02×105 Pa),但在180 ℃就开始升华。据此判断,氯化铝是共价化合物,可以证明该判断正确的实验依据是_____ (填字母序号)
A.AlCl3 可溶于水 B.AlCl3溶液可导电 C.熔化态的AlCl3不导电
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com