
| A. | 向稀盐酸中加入少量钠粒:2Na+2H2O→2Na++2OH-?+H2↑ | |
| B. | NaHSO4溶液与Ba(OH)2溶液混合呈中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | |
| C. | 用漂白粉溶液吸收尾气中SO2:Ca2++2ClO-+SO2+H2O→CaSO3↓+2HClO | |
| D. | 向含氯化铝的氯化镁溶液中加入氧化镁:2Al3++3MgO+3H2O=2Al(OH)3↓+3Mg2+ |
分析 A.不符合反应客观事实;
B.二者物质的量之比2:1反应恰好呈中性;
C.次氯酸根离子能够氧化二氧化硫;
D.铝离子水解生成氢离子,氢离子能够与氧化镁反应生成水和镁离子.
解答 解:A.向稀盐酸中加入少量钠粒,离子方程式:2Na+2H+→2Na++H2↑,故A错误;
B.NaHSO4溶液与Ba(OH)2溶液混合呈中性,离子方程式:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故B正确;
C.用漂白粉溶液吸收尾气中SO2,离子方程式:SO2+Ca2++ClO-+H2O=CaSO4↓+2H++Cl-,故C错误;
D.向含氯化铝的氯化镁溶液中加入氧化镁,离子方程式:2Al3++3MgO+3H2O=2Al(OH)3↓+3Mg2+,故D正确;
故选:BD.
点评 本题考查了离子方程式的书写,明确物质的性质及发生反应是解题关键,注意离子反应遵循客观事实、遵循原子个数、电荷数守恒规律,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳、甲烷、水汽等都是重要的温室气体 | |
| B. | 化学反应一定伴随能量变化,有能量变化也一定伴随化学反应 | |
| C. | 反应物所具有的总能量比生成物所具有的总能量高的反应是吸热反应 | |
| D. | Ba(OH)2•8H2O与NH4Cl的反应的△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 顺-2-丁烯和反-2-丁烯的加氢产物不同 | |
| B. | 甲醛、氯乙烯和乙二醇均可作为合成聚合物的单体 | |
| C. | ABS树脂、光导纤维及碳纤维都是有机高分子材料 | |
| D. | 酸性条件下,C2H5CO18OC2H5的水解产物是C2H5CO18OH和C2H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z、W简单离子半径大小关系:W>Z | |
| B. | X、Y、Z氢化物的稳定性强弱关系:X>Y>Z | |
| C. | X可与Y和Z分别形成共价化合物 | |
| D. | Y是活泼非金属,与W形成的化合物中不可能含共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 35Cl和37Cl中子数不同,所以它们的原子结构示意图、电子式、核外电子排布式、轨道表达式都不相同 | |
| B. | 两个不同原子的1s、2s、2p、3s、3P各亚层中电子的能量相同 | |
| C. | 短周期主族元素原子最外层电子数一定等于其最高化合价 | |
| D. | CO2通入Na2SiO3溶液中可以得到硅酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 +NaHCO3→
+NaHCO3→ +H2O+CO2↑;
+H2O+CO2↑; +3NaOH$→_{△}^{水}$
+3NaOH$→_{△}^{水}$ +NaCl+2H2O.
+NaCl+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
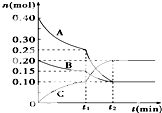 向10L的密闭容器中0.40mol A气体和0.20mol B气体,在一定条件下使其发生反应生成气体C,其物质的量的变化如图:
向10L的密闭容器中0.40mol A气体和0.20mol B气体,在一定条件下使其发生反应生成气体C,其物质的量的变化如图:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属性:X<W<Y<Z | |
| B. | X的简单阴离子和Z、W的简单离子均能促进水的电离 | |
| C. | 原子半径:Z<Y<W,而简单离子半径:W<Y<Z | |
| D. | Y的最高价氧化物对应的水化物与W的单质反应可制备X的单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100 mL 0.5 mol•L-1MgCl2溶液 | B. | 200 mL 0.25 mol•L-1AlCl3溶液 | ||
| C. | 50 mL 1 mol•L-1NaCl溶液 | D. | 25 mL 0.5 mol•L-1HCl溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com