
| A. | 乙酸乙酯、甘油、硝基苯 | B. | 乙醇、甘油、四氧化碳 | ||
| C. | 乙酸乙酯、苯、乙醇 | D. | 苯、四氯化碳、硝基苯 |
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案 期末好成绩系列答案
期末好成绩系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚溶液显弱酸性 | |
| B. | 苯酚比苯容易发生溴代反应 | |
| C. | 苯酚能与氢氧化钠溶液反应,而苯甲醇不能 | |
| D. | 苯酚和乙醇在60℃的水浴中,分别加入金属钠,苯酚中明显反应剧烈 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中Fe2+是还原剂,O2是还原产物 | |
| B. | 4 mol Na2O2在反应中共得到8NA个电子 | |
| C. | 每生成4 mol Fe(OH)3反应过程中共转移电子6 mol | |
| D. | 反应过程中可以看到白色沉淀转化为灰绿色再转化为红褐色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
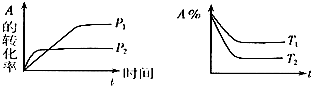
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S既作氧化剂又作还原剂 | B. | 消耗12gC时,反应转移5mol电子 | ||
| C. | 还原产物只有K2S | D. | KNO3只发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 半导体材料碳化硅 | B. | 超导材料铜锌合金 | ||
| C. | 透明陶瓷材料硒化锌 | D. | 超导材料Cs3C60 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液的pH=4 | |
| B. | 适当升高温度,溶液的pH不变 | |
| C. | 此酸的电离平衡常数约为1×10-7 | |
| D. | 由HX电离出的c(H+)约为水电离出的c(OH-)的106倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 序号 | 实验步骤 | 预期现象 | 结论 |
| 1 | |||
| 2 | 锥形瓶中液体含大量Br- | ||
| 3 | 锥形瓶中液体含大量H+ |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com