
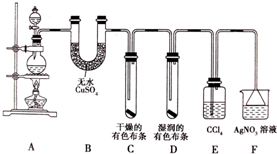
 某化学实验兴趣小组为探究实验室制备Cl2 的过程中有水蒸气和HCl挥发来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略):
某化学实验兴趣小组为探究实验室制备Cl2 的过程中有水蒸气和HCl挥发来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略):分析 加入条件下二氧化锰和浓盐酸反应生成氯气,也可用次氯酸钠和浓盐酸混合④KClO3和浓盐酸混合共热⑤KMnO4和浓盐酸混和,装置中无水硫酸铜用于吸收检验水,干燥的氯气不能使有色布条褪色,氯气和水反应生成次氯酸,D中湿润的有色布条褪色,E中四氯化碳吸收氯气,防止干扰F中氯化氢的检验,以此解答该题.
解答 解:加入条件下二氧化锰和浓盐酸反应生成氯气,也可用次氯酸钠和浓盐酸混合④KClO3和浓盐酸混合共热⑤KMnO4和浓盐酸混和,装置中无水硫酸铜用于吸收检验水,干燥的氯气不能使有色布条褪色,氯气和水反应生成次氯酸,D中湿润的有色布条褪色,E中四氯化碳吸收氯气,防止干扰F中氯化氢的检验,
(1)①MnO2和浓盐酸混合共热 ②MnO2、NaCl和浓硫酸混合共热③次氯酸钠和浓盐酸混合④KClO3和浓盐酸混合共热⑤KMnO4和浓盐酸混和.都是实验式常用制备氯气的方法,
故答案为:①②③④⑤;
(2)浓盐酸与足量MnO2反应制取Cl2,反应需要加热,氯化氢易挥发,反应消化氯化氢,随反应的不断进行浓盐酸的浓度逐渐变稀,稀盐酸不反应不与MnO2反应,
故答案为:浓盐酸的浓度随反应的不断进行逐渐变稀,变稀后将不再反应;
(3)①硫酸铜吸水生成蓝色硫酸铜晶体,检验含有水蒸气,故答案为:证明有水蒸气产生;白色固体变蓝色;
②干燥的有色布条不褪色,说明氯气不具有漂白性;湿润的有色布条褪色,氯气与水反应生成盐酸与次氯酸,盐酸不具有漂白性,所以使有色布条褪色的物质是次氯酸,故次氯酸漂白性,故答案为:氯气无漂白性,次氯酸有漂白性;
③用四氯化碳吸收氯气,防止干扰F中氯化氢的检验,故答案为:吸收氯气;
④氯化氢与硝酸银反应生成氯化银和硝酸,反应离子方程式为Ag++Cl-=AgCl↓,故答案为:Ag++Cl-=AgCl↓;
(4)氯气与水反应会生成盐酸,干扰F中氯化氢的检验,故在E、F之间加一装置,用碘化钾淀粉试液检验氯气是否被完全吸收,
故答案为:E与F;碘化钾淀粉试液.
点评 本题考查氯气的制取原理、实验装置评价与理解、氯气的性质、氯离子检验等,为高考常见题型,侧重于学生的分析能力和实验能力的考查,难度不大,关键是清楚实验的目的与原理.注意用可溶性固体氯化物和浓硫酸代替浓盐酸,原理是利用高沸点的酸制备挥发性酸,生成的硫酸盐应为可溶性盐.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
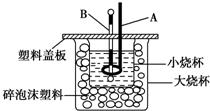 已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol.回答有关中和反应的问题.
已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol.回答有关中和反应的问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molNH3和 1molHCl混合 | |
| B. | 1mol NO和 0.5 molO2混合 | |
| C. | 1molSO2和 1 molH2S混合 | |
| D. | 等体积的NO和NO2被足量烧碱溶液吸收 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
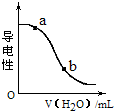
| A. | a点:c(H+)>c(CH3COO-)>c(OHˉ) | |
| B. | b点:c(H+)=c(CH3COO-)+c(OH-) | |
| C. | 已知常温下,物质的量浓度相等的CH3COONa与CH3COOH混合液的pH<7,在此溶液中继续加CH3COONa至pH=7,则此时溶液中存在:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-) | |
| D. | CH3COOH溶液的pH:a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4和C4H8 | B. | CH4和C3H6 | C. | C2H6和C3H6 | D. | C2H6和C4H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 32gO2和O3混合气体中含有原子总数为NA | |
| B. | 含有NA个Na+的Na2O溶于1L水中,Na+的物质的量浓度为2mol/L | |
| C. | 标准状况下,22.4L空气含有NA个单质分子 | |
| D. | 在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com