

分析 酸溶1步骤中加入硫酸、MnO2得到S,除锰步骤Mn2+转化成MnCO3沉淀,可知二氧化锰将CuS中-2价的S氧化为硫单质,溶液中CuSO4转变为[Cu(NH3)4]CO3留在溶液中,蒸氨步骤中[Cu(NH3)4]CO3发生分解反应得到CuO固体、氨气与二氧化碳,再用硫酸溶解CuO得到CuSO4,与氯化钠、亚硫酸钠反应得到CuCl与硫酸钠,发生反应:2Cu2++2Cl-+SO32-+H2O=2CuCl↓+SO42-+2H+,经过过滤、洗涤、干燥得到CuCl,滤液中含有硫酸钠、硫酸.洗涤时,应避免CuCl溶解损失,根据溶解平衡,可以先用盐酸洗涤.
解答 解:酸溶1步骤中加入硫酸、MnO2得到S,除锰步骤Mn2+转化成MnCO3沉淀,可知二氧化锰将CuS中-2价的S氧化为硫单质,则加入硫酸生成硫酸铜、硫酸锰以及S,反应的化学方程式为CuS+MnO2+2H2SO4=CuSO4+MnSO4+S+2H2O.
故答案为:CuS+MnO2+2H2SO4=CuSO4+MnSO4+S+2H2O.
点评 本题考查物质制备实验、对工艺流程分析评价、条件的控制、物质的分离提纯等,理解工艺流程原理是解题关键,是对学生综合能力的考查,难度中等.


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应放出a kJ热量 | |
| B. | X和Y的物质的量之比为1:2 | |
| C. | 反应物和生成物的浓度都不再发生变化 | |
| D. | X的正反应速率等于Z的逆反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NA个CO2分子中含1mol氧原子 | |
| B. | 3.2g S2-的核外电子数1.6NA | |
| C. | 1 mol•L-1Na2CO3溶液中含有2NA个Na+ | |
| D. | 1个H2SO4分子中氧原子的质量为64/NAg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定有一种元素被氧化,另一种元素被还原 | |
| B. | 在反应中应有沉淀、气体或水生成 | |
| C. | 置换反应一定属于氧化还原反应 | |
| D. | 化合反应和复分解反应有可能是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 漂白粉露置在空气中:ClO-+CO2+H2O═HClO+HCO3- | |
| B. | 用少量氨水吸收二氧化硫:SO2+NH3•H2O=HSO3-+NH4+ | |
| C. | 少量CO2通入苯酚钠溶液:2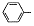 +CO2+H2O→2 +CO2+H2O→2 OH+CO32- OH+CO32- | |
| D. | 磁性氧化铁(Fe3O4)溶于氢碘酸:Fe3O4+8H+═Fe2++2Fe3++4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有大量Fe3+的溶液中:Na+、SCN-、Cl-、Br- | |
| B. | 与铝粉反应放出氢气的无色溶液中:NO3-、Al3+、Na+、SO42- | |
| C. | AlO2-、Cl-、Al3+、K+ | |
| D. | 在由水电离出的c(H+)=1.0×10-12mol/L的溶液中:CO32-、Na+、K+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | E是一种非金属元素 | B. | 在ECln中E与Cl之间形成共价键 | ||
| C. | E的一种氧化物为EO | D. | E位于元素周期表的ⅡA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.37 mol | B. | 1.5 mol | C. | 0.63 mol | D. | 0.74 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com