
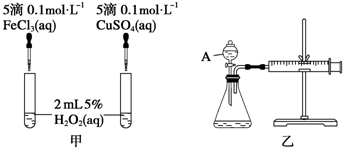
 �����dzµ��㡱������Ϊ���ڴ������������������ζ��������������ʵ�������ǿ�������ͼ��ʾ��װ����ȡ����������
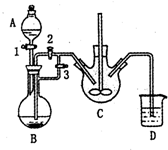
�����dzµ��㡱������Ϊ���ڴ������������������ζ��������������ʵ�������ǿ�������ͼ��ʾ��װ����ȡ�������������� ��1��������Ӧ�ı���Ϊ�����ǻ��������⣬�÷�Ӧ��������������ˮ����Ϊ���淴Ӧ��
��2������̼������Һ�����ᷴӦ��ȥ���ᡢͬʱ���������������ܽ�ȣ����ڷֲ㣻
��3����������Һ���¿��ܷ���������
��4�����뻥�����ܵ�Һ�壬���÷�Һ�ķ������룬����������̼������Һ�ֲ㣻
��5�����뼸�����Ƭ���ɷ�ֹҺ����ҷ��ڣ�
��� �⣺��1���������Ҵ�����������Ӧ����������������ȡ���������Ļ�ѧ����ʽΪCH3COOH+C2H5OH$?_{��}^{ŨH_{2}SO_{4}}$CH3COOC2H5+H2O��
�ʴ�Ϊ��CH3COOH+C2H5OH$?_{��}^{ŨH_{2}SO_{4}}$CH3COOC2H5+H2O��
��2���Ʊ���������ʱ���ñ���̼������Һ��Ŀ�����кͻӷ����������ᣬʹ֮ת��Ϊ����������ˮ�У�������������������ζ���ܽ�ӷ��������Ҵ�����������������ˮ�е��ܽ�ȣ����ڷֲ�õ�����
�ʴ�Ϊ����ȥ��������Ҵ������������������ܽ�ȣ�
��3�����ܲ��ڱ���̼������Һ��Һ���¿��ܷ�����������װ����ͨ�����ĵ���Ҫ���ڱ���̼������Һ��Һ���ϣ����ܲ�����Һ�У�ԭ���Ƿ�ֹ������
�ʴ�Ϊ����ֹ������
��4��������������ʱ�Ƚ�ʢ�л������Թܳ�����ñ���̼������Һ�кͻӷ����������ᣬʹ֮ת��Ϊ����������ˮ�У��ܽ�ӷ��������Ҵ�����������������ˮ�е��ܽ�ȣ����÷ֲ��Һ���ϲ�Ϊ������������֪�Ƶõ������������������Ӧ���õ�ʵ������Ƿ�Һ���ʴ�Ϊ����Һ��
��5������ʵ��ʱ����ʱ����ʢ������������Թ�����뼸�����Ƭ����Ŀ���Ƿ�ֹ���У��ʴ�Ϊ����ֹ���У�
���� ���⿼���л�����Ʊ�ʵ�飬Ϊ��Ƶ���㣬�����Ʊ�ʵ��ԭ����ʵ��װ�õ����á�ʵ�鼼�ܡ��������뷽��Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ˮ������ˮ�м�����������ʹ��ˮ���� | |
| B�� | ���ӽ���Ĥ�ڹ�ҵ��Ӧ�ù㷺�����ȼҵ��ʹ�������ӽ���Ĥ | |
| C�� | ������һ�������Խ�ǿ�����壬����������ˮ������ | |
| D�� | SO2���л�ԭ�ԣ�������֪Ũ�ȵ�KMnO4��Һ�ⶨʳƷ��SO2������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
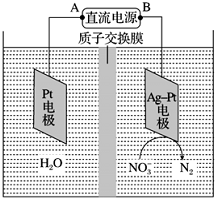 �绯ѧ����NO3-��ԭ����ͼ��ʾ��
�绯ѧ����NO3-��ԭ����ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
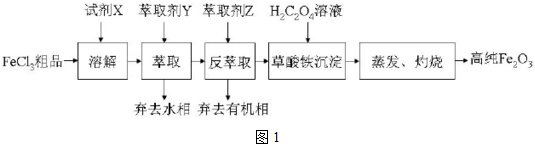
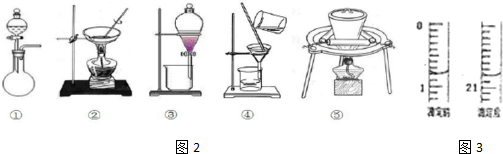
 ����������[CH3CH��OH��COO]2Fe•3H2O��Mr=288����һ�ֳ��õIJ���������ͨ��������̼��������Ӧ�Ƶã�
����������[CH3CH��OH��COO]2Fe•3H2O��Mr=288����һ�ֳ��õIJ���������ͨ��������̼��������Ӧ�Ƶã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeCl2 | B�� | CuS | C�� | NO2 | D�� | SO2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com